
如图图表示各物质之间的转化关系.

已知:
(1)A是无色液体,L是不溶于稀硝酸的白色沉淀,E、F、H、J、X、Y和Z都是气体;
(2)G、X、Y和Z都是单质,其它是化合物,其中Y呈黄绿色,H呈红棕色,E和F都极易溶解于水,二者相遇会有白烟生成.
(3)B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且价态也相同,B中非金属元素的质量分数为28%,组成B的金属元素原子核外的K层和M层电子数相同.
请根据以上信息完成下列要求:
(1)写出下列物质的化学式:C ,F ,H
(2)写出E的电子式
(3)实验室制Y的离子方程式为
(4)上述反应中是氧化还原反应的除了②、③、④和⑦外,还有(填反应代号)
(5)写出反应①④⑤的化学反应方程式
①
④
⑤
(6)保持容器的温度和体积不变,在反应③刚好完全反应时,反应前后容器的压强之比为 .
考点: 无机物的推断.
分析: 气体单质Y呈黄绿色,则Y为Cl2,气体化合物H呈红棕色,则H为NO2,气体化合物E和F都极易溶解于水,二者相遇会有白烟生成,应分别为NH3、HCl中的一种,由反应③可知,E为NH3,F为HCl,气体单质X为N2,B是由一种金属与一种非金属元素组成的化合物,组成B的金属元素原子核外的K层和M层电子数相同,则金属元素为Mg,A为无色液体,结合反应①可知,A为H2O、B为Mg3N2,B中N元素的质量分数为28%,则D为Mg(OH)2.E(NH3)与气体单质Z反应生成气体化合 J与A(水),J与Z反应得到H(NO2),则Z为O2、J为NO,由反应⑦可知W为HNO3,反应⑥中I与F(HCl)反应得到W(硝酸)与L,且L是不溶于稀硝酸的白色沉淀,则I为AgNO3,L为AgCl.反应④中单质G与W(硝酸)反应得到硝酸银、水、二氧化氮,则G为Ag,C中N元素化合价与B中相同,即N元素为﹣3价,结合反应②可知C为Ag3N,据此解答.
解答: 解:气体单质Y呈黄绿色,则Y为Cl2,气体化合物H呈红棕色,则H为NO2,气体化合物E和F都极易溶解于水,二者相遇会有白烟生成,应分别为NH3、HCl中的一种,由反应③可知,E为NH3,F为HCl,气体单质X为N2,B是由一种金属与一种非金属元素组成的化合物,组成B的金属元素原子核外的K层和M层电子数相同,则金属元素为Mg,A为无色液体,结合反应①可知,A为H2O、B为Mg3N2,B中N元素的质量分数为28%,则D为Mg(OH)2.E(NH3)与气体单质Z反应生成气体化合 J与A(水),J与Z反应得到H(NO2),则Z为O2、J为NO,由反应⑦可知W为HNO3,反应⑥中I与F(HCl)反应得到W(硝酸)与L,且L是不溶于稀硝酸的白色沉淀,则I为AgNO3,L为AgCl.反应④中单质G与W(硝酸)反应得到硝酸银、水、二氧化氮,则G为Ag,C中N元素化合价与B中相同,即N元素为﹣3价,结合反应②可知C为Ag3N.
(1)根据上面的分析可知,C为Ag3N,F为HCl,H为NO2,故答案为:Ag3N;HCl;NO2;
(2)E为NH3,电子式为: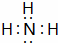 ,故答案为:
,故答案为: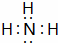 ;
;
(3)Y为Cl2,实验室制Y的离子方程式为MnO2+4H++2Cl﹣ Mn2++2H2O+Cl2↑,故答案为:MnO2+4H++2Cl﹣
Mn2++2H2O+Cl2↑,故答案为:MnO2+4H++2Cl﹣ Mn2++2H2O+Cl2↑;
Mn2++2H2O+Cl2↑;
(4)上述反应中除①⑧外均为氧化还原反应,氧化还原反应中除了②、③、④和⑦外,还有⑤⑥,故答案为:⑤⑥;
(5)反应①的化学反应方程式:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;
反应④的化学反应方程式:Ag+2HNO3(浓)=AgNO3+NO2↑+H2O;
反应⑤的化学反应方程式:4NH3+5O2 4NO+6H2O,
4NO+6H2O,
故答案为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;Ag+2HNO3(浓)=AgNO3+NO2↑+H2O;4NH3+5O2 4NO+6H2O;
4NO+6H2O;
(6)反应③的化学方程式为:2NH3+3Cl2=N2+6HCl,保持容器的温度和体积不变,刚好完全反应时,反应前后气体的物质的量之比为5:7,所以反应前后容器的压强之比为5:7,
故答案为:5:7.
点评: 本题考查无机物推断,物质的颜色、状态及特殊反应为推断突破口,需要学生熟练掌握元素化合物知识,难度中等.


科目:高中化学 来源: 题型:
下列有关化学研究的正确说法是( )
|
| A. | 同时改变两个变量来研究反映速率的变化,能更快得出有关规律 |
|
| B. | 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
|
| C. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
|
| D. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是利用丙烯和对二甲苯合成有机高分子材料W的转化关系示意图.
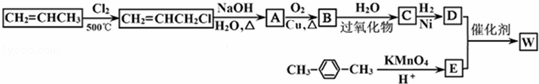
已知:①C不含甲基,B可以发生银镜反应,1molD与足量钠可生成22.4L H2(标准状况下).
①R﹣CH=CH2+H2O R﹣CH2CH2OH
R﹣CH2CH2OH
②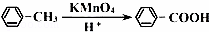
请完成下列各问:
(1)A的结构简式是 ,D的核磁共振氢谱图中有 个峰.
(2)C中所含官能团的名称 、 .
(3)C→D反应类型为 .
(4)有关物质B所具有的性质的叙述中正确的是(填序号) .
a.能发生银镜反应 b.能使溴水褪色 c.能发生酯化反应 d.可发生聚合反应
(5)写出下列反应的化学方程式:
①A→B: .
②D+E→W: .
③D的同分异构体(同一个碳原子上连接两个﹣OH的不能稳定存在)和E的同分异构体反应生成最小环酯: .
(6)物质E有多种同分异构体,请分别写出满足以下条件一个E的同分异构体的结构简式:
ⅰ.①遇FeCl3溶液显紫色 ②可发生银镜反应 ③能发生水解反应 .
ⅱ.①遇FeCl3溶液显紫色 ②可发生银镜反应 ③能和NaHCO3发生反应生成CO2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质与应用均正确的是( )
A. SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力
B. Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C. 氨气是一种碱性气体,可用碱石灰或无水CaCl2干燥
D. MgO的熔点很高,可用于制作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、HCO3﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,下列说法正确的是( )

A. d点溶液中含有的溶质只有Na2SO4
B. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
C. ab段发生的离子反应为:Al3++3OH﹣=Al(OH)3↓,Mg2++2OH﹣=Mg(OH)2↓
D. 原溶液中含有的阳离子必定有H+、NH4+、Al3+,但不能肯定Mg2+和Fe3+中的哪一种
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生做乙醛还原性的实验,取1 mol·L-1的CuSO4溶液2 mL和0.4 mol·L-1的NaOH溶液4 mL,在一个试管内混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无砖红色沉淀,实验失败的原因是( )
A.NaOH不足量 B.CuSO4不足量
C.乙醛溶液太少 D.加热时间不够
查看答案和解析>>
科目:高中化学 来源: 题型:
今有以下几种化合物
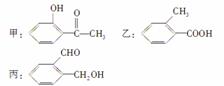
(1)请写出丙中含氧官能团的名称:
________________________________________________________________________。
(2)请判别上述哪些化合物互为同分异构体:
________________________________________________________________________
____________。
(3)请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可)。
①鉴别甲的方法:
________________________________________________________________________;
②鉴别乙的方法:
________________________________________________________________________;
③鉴别丙的方法:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
青苹果汁遇碘溶液显蓝色,熟苹果汁能还原银氨溶液,这说明( )
A.青苹果中只含淀粉不含糖类 B.熟苹果中只含糖类不含淀粉
C.苹果转熟时淀粉水解为单糖 D.苹果转熟时单糖聚合成淀粉
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,H2(g)+CO2(g)⇌H2O(g)+CO(g) 的平衡常数K=2.25.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )

A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com