
某研究小组对“Br2和I2能否将Fe2+氧化为Fe3+”这一课题进行实验和探究。请你完成相关问题的回答。
(1)提出合理的假设
假设1: Br2和I2都可以将Fe2+氧化为Fe3+;
假设2: Br2和I2都不能将Fe2+氧化为Fe3+;
假设3:
(2)实验验证
在大试管中加适量铁粉,加入10 mL 稀硫酸,振荡试管,充分反应后,铁粉有剩余,将所得的FeSO4溶液稀释到200mL,备用。
实验Ⅰ:向试管1中加入2 mL浅绿色的 FeSO4溶液,再滴加少量红棕色的溴水,振荡试管,溶液为黄色;
实验Ⅱ:向试管2中加入2 mL浅绿色的 FeSO4溶液,再滴加少量棕黄色的碘水,振荡试管,溶液为黄色。
(3)对实验现象的分析与讨论
①甲同学认为实验Ⅰ的现象说明溴水能将Fe2+氧化,离子方程式为 。
②乙同学认为应该补充实验,才能得出甲的结论。乙的实验操作以及预期现象是 。
③该小组同学对实验Ⅱ中溶液呈黄色的原因展开了讨论:
可能1:碘水与 FeSO4溶液不反应,黄色是碘水稀释后的颜色。
可能2: 。
丙同学和丁同学分别设计了以下实验方案以确定可能的原因。
丙方案:向试管2所得溶液中继续加入0.5mLCCl4,充分振荡,静置一段时间后。取出上层溶液,滴加几滴KSCN 溶液;
丁方案:向试管2所得溶液中继续加入加入0.5mL乙酸乙酯,充分振荡,静置一段时间后。取出下层溶液,滴加几滴KSCN 溶液;
你认为 方案为最佳方案,理由是 。
(4)拓展延伸
①为准确测定此实验所用的FeSO4溶液的浓度,某同学补充了以下实验:
滴定:量取20.00mL稀释后得到的溶液于锥形瓶中,将0.0200mol/LKMnO4标准溶液装入50mL中,滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4溶液V mL。
②计算:此实验中所用的FeSO4溶液的物质的量浓度= mol/L(要求只列出算式,不需运算)。
(已知反应式:Fe2+ + MnO4- +H+ — Fe3+ + Mn2+ + H2O,未配平)
(1)假设3:Br2能将Fe2+氧化为Fe3+而I2不能(2分)
(3)①2Fe2++Br2=2Fe3++2Br-(2分)
②取少量实验Ⅰ的黄色溶液于试管中,滴加几滴KSCN溶液,振荡,溶液变为红色。(3分)
③可能2:碘水与FeSO4溶液发生反应生成Fe2(SO4)3, Fe2(SO4)3溶液也是黄色的,所以溶液的颜色没有明显的变化。(2分,表述合理给分)丁(2分);理由:亚铁离子与空气接触容易被氧化,丁方案中加入乙酸乙酯既可作为萃取剂又能起到液封的作用,减少空气对实验的影响。(3分,表述合理给分)
(4)①酸式滴定管(1分)②0.0200×V×10-3×5 /(20×10-3)或0.0200×V×5 /20(2分)
【解析】
试题分析:(1)根据前两个假设,结合溴与碘的氧化性 的强弱,提出第三个假设:Br2能将Fe2+氧化为Fe3+而I2不能;
(3)①溴氧化亚铁离子为铁离子,本身被还原成溴离子,离子方程式为2Fe2++Br2=2Fe3++2Br-
②需要补充的实验目的是验证铁离子的存在,所以取少量实验Ⅰ的黄色溶液于试管中,滴加几滴KSCN溶液,振荡,溶液变为红色,说明溴水能将Fe2+氧化;
③可能2是碘水与 FeSO4溶液反应生成硫酸铁,铁离子的颜色也为黄色;丁方案更合理,因为乙酸乙酯的密度比水小,且不溶于水,在溶液的上层,可以起到隔绝空气的作用,防止亚铁离子被空气中的氧气氧化;同时还起到萃取的作用,碘在有机溶剂中的溶解度大于在水中的溶解度,所以萃取后向下层液体中滴加KSCN溶液,判断有无铁离子生成;
(4)①酸性高锰酸钾溶液的氧化性强所以用酸式滴定管装酸性高锰酸钾溶液;②根据得失电子守恒,亚铁离子与高锰酸根离子之间的物质的量比例关系为5Fe2+~MnO4-,所以硫酸亚铁的浓度为0.0200×V×10-3×5 /(20×10-3)mol/L。
考点:考查对实验的设计、判断、分析能力,氧化还原反应的计算


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源:2013-2014学年广东省潮州市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
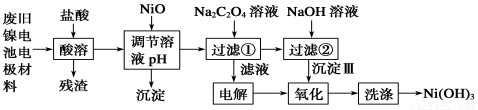
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。②K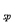 (Ni(OH)
(Ni(OH) ): 5.0×10-16 , K
): 5.0×10-16 , K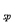 (NiC2O4): 4.0×10-10
(NiC2O4): 4.0×10-10
回答下列问题:
(1)酸溶后所留残渣的主要成份 (填物质名称)。
(2)用NiO调节溶液的pH,析出沉淀的成分为____________________(填化学式);用pH试纸测定某溶液pH的具体操作是 。
(3)写出加入Na2C2O4溶液后反应的化学方程式_____________________________。
(4)写出加入NaOH溶液所发生反应的离子方程式 ,该反应的平衡常数为 。
(5)沉淀Ⅲ可被电解所得产物之一 (填化学式)氧化生成Ni(OH)3 ,如何洗涤Ni(OH)3 沉淀?
。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标况下,11.2L乙烷中含有共价键的数目为3NA
B.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2NA
C.常温下,22.4L甲烷中含有的电子数为10NA
D.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.常温常压下,1.7gH2O2中含有的电子数为0.9NA
B.1 mol.L-1CuCl2溶液含有2NA个Cl-
C.1 mol Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子
D.标准状况下,2.24L戊烷所含分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省广州市毕业班综合测试(二)理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、R的原子序数依次增大,X单质在暗处与H2剧烈化合并发生爆炸,Y位于第IA族,Z所处的周期序数与族序数相等,W元素最高正价与最低负价之和为0,R与X同族,则
A.原子半径:Z>Y>X
B.X与R的核电荷数相差18
C.气态氢化物稳定性:W>R
D.Y与Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省十校联考高三下学期理综化学试卷(解析版) 题型:选择题
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法不正确的是
元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
化合价 | -3 | -2 | +1 | -4 | -1 |
A.丙的常见氧化物有两种
B.气态氢化物稳定性:甲>乙
C.丁的氧化物能与戊的氢化物的水溶液反应
D.原子半径大小:甲<丙
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省枣庄市高三下学期第二次模拟考试理综化学试卷(解析版) 题型:填空题
已知:苯和卤代烃在催化剂作用下可以生成烷基苯和卤化氢。根据以下转化关系(生成物中所有无机物均已略去),回答下列问题:
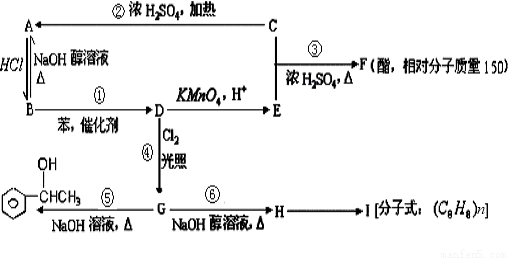 。
。
(1)D的结构简式为 ,E、H中所含官能团的名称分别是 、 。
(2)①②③④⑤⑥反应中属于消去反应的是 。
(3)写出⑥的反应方程式 。
写出H→I的反应方程式 。
(4)简述验证G中含有氯元素的方法是 。
(5)写出一种符合下列要求的F的同分异构体的结构简式;
①F的同分异构体中属于酯类,能发生银镜反应,且苯环上的一氯取代物只有两种: 。
②F的同分异构体中属于醇类,能发生银镜反应,且苯环上的一氯取代物只有两种: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省文登市高三第三次统考理科综合化学试卷(解析版) 题型:选择题
下列说法正确的是(N A表示阿伏加德常数)
A.1molCu与足量硫反应生成Cu2S,转移的电子数为2 N A
B.R2+的质量数为A,中子数为N,则ngR该价态的氧化物中含质子数为 N A
N A
C.氯化铁生成Fe(OH)3 胶体的离子方程式:Fe3++3H2O =Fe(OH)3↓+3H+
D.在加入铝片能生成氢气的溶液中一定共存的离子组:Na+、Ba2+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京顺义区高三第二次统练理综化学试卷(解析版) 题型:选择题
第三周期元素,浓度均为0.01 mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示。则下列说法正确的是

A.气态氢化物的稳定性:N>R
B.Z的最高价氧化物对应的水化物能溶于稀氨水
C.Y和R形成的化合物既含离子键又含共价键
D.X和M两者最高价氧化物对应的水化物反应后溶液的pH>7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com