
下列实验操作能达到目的是( )
|
| A. | 用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体 |
|
| B. | 蒸干并灼烧AlCl3溶液可获得Al(OH)3固体 |
|
| C. | 用Na2S溶液和CuSO4溶液反应制取CuS固体 |
|
| D. | 蒸发MgCl2溶液制取MgCl2固体 |
考点:
盐类水解的应用.
专题:
盐类的水解专题.
分析:
A、硫离子水解呈碱性,铝离子水解呈酸性,二者溶液混合水解相互促进生成氢氧化铝和硫化氢;
B、氯化铝溶液中铝离子水解生成氢氧化铝和氯化氢,蒸发溶液挥发氯化氢得到水解产物氢氧化铝,灼烧得到氧化铝;
C、硫离子和铜离子结合生成硫化铜沉淀,不溶于酸;
D、氯化镁水解生成氢氧化镁和盐酸,蒸干氯化氢挥发得到水解产物,得不到氯化镁.
解答:
解:A、硫离子水解呈碱性,铝离子水解呈酸性,二者溶液混合水解相互促进生成氢氧化铝和硫化氢,3S2﹣+2Al3++6H2O=2Al(OH)3↓+3H2S,不能制取Al2S3固体,故A错误;
B、氯化铝溶液中铝离子水解生成氢氧化铝和氯化氢,蒸发溶液挥发氯化氢得到水解产物氢氧化铝,灼烧得到氧化铝;Al3++3H2O⇌Al(OH)3↓+3H+,2Al(OH)3=Al2O3+3H2O,故B错误;
C、用Na2S溶液和CuSO4溶液反应制取CuS固体不溶于水和酸,故C正确;
D、氯化镁水解生成氢氧化镁和盐酸,蒸干氯化氢挥发得到水解产物,得不到氯化镁,故D错误;
故选C.
点评:
本题考查了盐类水解的应用,主要是蒸干溶液产物的判断,题目难度中等.


科目:高中化学 来源: 题型:
下面食谱营养搭配最均衡的是( )
|
| A. | 凉拌青菜、土豆丝、馒头 |
|
| B. | 糖醋排骨、清蒸鲈鱼、米饭 |
|
| C. | 虾仁白菜、红烧带鱼、酸菜炖猪蹄、萝卜汤 |
|
| D. | 酱牛肉、炒油菜、红烧豆腐、西红柿蛋汤、馒头 |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃,水的电离达到平衡:H2O⇌H++OH﹣,下列叙述正确的是( )
|
| A. | 向水中加入稀醋酸,平衡逆向移动,c(H+)降低 |
|
| B. | 向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaSO3(s)⇌Ba2+(aq)+SO32﹣ (aq)平衡体系中,下列措施可使沉淀量减少的是( )
|
| A. | 加入K2SO3(s) | B. | 加入稀HNO3 | C. | 加入稀盐酸 | D. | 加入K2SO4(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
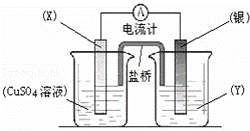
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极.
查看答案和解析>>
科目:高中化学 来源: 题型:
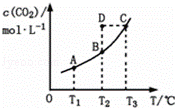
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)⇌CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )
|
| A. | 反应CO(g)+H2O(g)⇌CO2(g)+H2(g)的△H>0 |
|
| B. | 在T2时,若反应处于状态D,则一定有ν正<ν逆 |
|
| C. | 平衡状态A与C相比,平衡状态A的c(CO)小 |
|
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com