
| A£®Ī»ÓŚÖÜĘŚ±ķÖŠĖÄÖÜĘŚ¢ų×å | B£®Ö»ÓŠ2øö ¼Ūµē×Ó ¼Ūµē×Ó |
| C£®+3¼ŪĄė×Ó±Č+2¼ŪĄė×ÓµÄŃõ»ÆŠŌĒæ | D£®Ę䵄֏ÄŃČÜÓŚÅØĻõĖį |
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| µēĄėÄÜ/kJ”¤mol”Ŗ1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
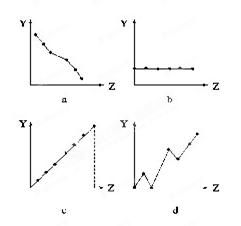
 ŌŖĖŲÓŠ¹ŲµÄŠŌÖŹĻą·ūµÄĒśĻß±źŗÅĢīČėĻąÓ¦µÄæÕøńÖŠ£ŗ
ŌŖĖŲÓŠ¹ŲµÄŠŌÖŹĻą·ūµÄĒśĻß±źŗÅĢīČėĻąÓ¦µÄæÕøńÖŠ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ō×Ó°ė¾¶“óŠ”ĪŖ£ŗY > Z > X |
| B£®YÓėZŠĪ³ÉµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ |
| C£®ČōYĪŖ½šŹōŌŖĖŲ£¬ŌņXŅ²ĪŖ½šŹōŌŖĖŲ |
| D£®ČōZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŹĒĒæĖį£¬ŌņYŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¾ßÓŠĮ½ŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ¢Ł | | | | | | | | | | | | | | | | | |
| | ¢Ś | | | | | | | | | | | | ¢Ū | | | | |
| | ¢Ü | | | | | | | | | | | ¢Ż | | ¢Ž | | ¢ß | |
| | ¢ą | | | | | | | |  | ¢į | | | | | | | |
 ӣ
”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®16”¢16”¢16 | B£®18”¢16”¢16 | C£®18”¢18”¢16 | D£®16”¢16”¢18 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®13CÓė15NÓŠĻąĶ¬µÄÖŠ×ÓŹż | B£®13CÓėC60»„ĪŖĶ¬ĖŲŅģŠĪĢå |
| C£®15NÓė14N»„ĪŖĶ¬Ī»ĖŲ | D£®15NµÄŗĖĶāµē×ÓŹżÓėÖŠ×ÓŹżĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 µÄŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©___________________________________”£
µÄŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©___________________________________”£²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com