
| A、4℃时,5.4mL水中所含的水分子数是0.3NA(4℃时,水的密度为1.0g/ml) |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为 NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |
| m |
| M |
| 5.4g |
| 18g/mol |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
A、2NaCl(水溶液)
| ||
B、CuO+H2
| ||
C、Fe3O4+4CO
| ||
D、2HgO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(s)+O2(g)═CO(g)△H=-110.5 kJ/mol | ||
| B、C(s)+O2(g)═CO2(g)△H=-393.5 kJ/mol | ||
| C、2H2 (g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | ||
D、H2(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g氮气所含有的原子数目为NA |
| B、化学反应中1mol金属镁变成镁离子时失去电子数目为2NA |
| C、标准状况下,22.4L水中含有个水分子NA |
| D、标准状况下,22.4L氯化氢所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、25℃时,56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
| C、常温下,1.20 g NaHSO4固体中含有的阴阳离子总数为0.3 NA |
| D、78 g Na2O2和Na2S的混合物中含有的阴离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.6g 由NO2和N2O4组成的混合物中含有氧原子的数目为 0.2NA |
| B、1 mol Na2O2固体中含离子总数为4NA |
| C、标准状况下,1.12LCCl4含有C-Cl键的数目为0.2NA |
| D、将0.1mol FeCl3溶于 1L水中,所得溶液中含有0.1NA个Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
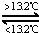 Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )
Sn(s、白)△H3=+2.1kJ/mol,下列说法正确的是( )| A、△H1>△H2 |
| B、锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 |
| C、锡在常温下以灰锡状态存在 |
| D、灰锡转化为白锡的反应是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com