
【题目】铜阳极泥(主要含有铜、银、金、少量的镍)是有色金属冶炼过程中重要的“二次资源”。其合理处理对于实现资源的综合利用具有重要意义。一种从铜阳极泥中分离提取多种金属元素的工艺流程如下:

已知:分金液的主要成分为[AuCl4]-;分金渣的主要成分为AgCl;分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-=Ag++2SO32-
(1)“分铜”时,单质铜发生反应的化学方程式为___________,已知“分铜”时各元素的浸出率如下表所示。

“分铜”时加入足量的NaC1的主要作用为______________________。
(2)“分金”时,单质金发生反应的离子方程式为______________________。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。

“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgC的原因为___________。调节溶液的pH不能过低,理由为___________。
(4)已知离子浓度≤10-5mol/L时,认为该离子沉淀完全。已知: Ksp[Pb(OH)2]=2.5×10-16,Ksp[Sb(OH)3]=10-41。浸取“分银渣”可得到含0.025 mol/L Pb2+的溶液(含少量Sb3+杂质)。欲获得较纯净的Pb2+溶液,调节PH的范围为___________。(忽略溶液体积变化)
(5)工业上,用镍为阳极,电解0.1 mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:

为获得髙纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为___________g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为___________。
【答案】Cu+H2O2+H2SO4=CuSO4+2H2O 使溶解出的Ag+形成AgCl进入分铜渣,避免银元素的损失 2Au+ClO3-+7Cl-+6H+=2[AuCl4]- +3H2O 分银液中存在[Ag(SO3)2]3![]() Ag++2SO32-,加H2SO4至pH=4,SO32-转化为HSO3-,c(SO32-)减小,平衡正向移动,c(Ag+)增大,Ag+与分银液中Cl-反应生成AgCl, 避免产生污染气体SO2 2≤pH<7 10 H2
Ag++2SO32-,加H2SO4至pH=4,SO32-转化为HSO3-,c(SO32-)减小,平衡正向移动,c(Ag+)增大,Ag+与分银液中Cl-反应生成AgCl, 避免产生污染气体SO2 2≤pH<7 10 H2
【解析】
本题是结合工艺流程考查元素化合物知识的综合应用。
铜阳极泥加入硫酸、过氧化氢和氯化钠进行“分铜”,“分铜”时,单质铜发生反应是铜在酸性溶液中被过氧化氢氧化生成硫酸铜和水,“分铜”时加人足量的NaCl的主要作用为使溶解出的Ag+形成AgCl进入分铜渣,加入盐酸和氯酸钠分金,分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,分金渣加入亚硫酸钠过滤得到分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-加入硫酸沉银,促使[Ag(SO3)2]3-Ag++2SO32-平衡正向移动,电离出Ag+,Ag+与分银液中的Cl-反应生成AgCl。
(1)①“分铜”时,单质铜发生反应是铜在酸性溶液中被过氧化氢氧化生成硫酸铜和水;
②“分铜”时加人足量的NaCl沉淀银离子,避免银的损失;
(2)分金液的主要成分为[AuCl4]-,“分金”时,单质金发生反应是金和加入的氯酸钠和盐酸发生氧化还原反应生成[AuCl4]-,据此书写离子方程式;
(3)①分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-Ag++2SO32-,H2SO4电离出的H+降低了SO32-的浓度,平衡正向进行;
②调节溶液的PH 不能过低,容易和亚硫酸根离子反应生成污染性气体二氧化硫;
(4)根据Ksp[Pb(OH)2]可计算出Pb2+离子开始出现沉淀时的pH值,根据Ksp[Sb(OH)3]]可计算出Sb3+离子沉淀完全时的pH值,据此判断溶液的pH值范围。
(1)“分铜”时,单质铜发生反应的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O。“分铜”时加入足量的NaC1的主要作用是使溶解出的Ag+形成AgCl进入分铜渣,避免银元素的损失。本小题答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;使溶解出的Ag+形成AgCl进入分铜渣,避免银元素的损失。
(2)“分金”时,单质金发生反应的离子方程式为2Au+ClO3-+7Cl-+6H+=2[AuCl4]- +3H2O。本小题答案为:2Au+ClO3-+7Cl-+6H+=2[AuCl4]- +3H2O。
(3)“沉银”时,需加入硫酸调节溶液的pH=4,是因为H2SO4电离产生的氢离子降低了SO32-的浓度,促使[Ag(SO3)2]3![]() Ag++2SO32-平衡正向移动,产生Ag+,Ag+与分银液中Cl-反应生成AgCl;调节溶液的pH不能过低,避免产生污染气体SO2。
Ag++2SO32-平衡正向移动,产生Ag+,Ag+与分银液中Cl-反应生成AgCl;调节溶液的pH不能过低,避免产生污染气体SO2。
(4)欲获得较纯净的Pb2+溶液,则Pb2+的浓度为0.025 mol/L,Ksp[Pb(OH)2]=c(Pb2+)c2(OH-)=0.025 mol/L×c2(OH-)=2.5×10-16,故c(OH-)=1.0×10-7,pH<7
(5)根据图可知,阴极电流效率和镍的成粉率达到最大,NH4Cl的浓度为10g/L;根据电解原理,阴极电极反应为2H++2e-=H2↑,则阴极产生的气体是H2。本小题答案为:10;H2。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一体积可变的容器中进行。下列条件的改变对其化学反应速率几乎没有影响的是:①增加C的用量;②将容器体积缩小一半;③保持容器体积不变,充入氮气使容器内压强增大;④保持压强不变,充入氮气使容器的体积变大
CO(g)+H2(g)在一体积可变的容器中进行。下列条件的改变对其化学反应速率几乎没有影响的是:①增加C的用量;②将容器体积缩小一半;③保持容器体积不变,充入氮气使容器内压强增大;④保持压强不变,充入氮气使容器的体积变大
A. ②④ B. ①③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)与氢气或与水在催化剂作用下的反应如下:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △H1=-17kJ/mol;
H2S(g)+CO(g) △H1=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)两个反应在热力学上趋势均不大,其原因是:________________。
(2)反应CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=_______。
H2(g)+CO2(g)的△H=_______。
(3)羰基硫、氢气、水蒸气共混体系初始投料比不变,提高羰基硫与水蒸气反应的选择性的关键因素是______。
(4)在充有催化剂的恒压密闭容器中只进行反应Ⅰ![]() 设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示:
设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示:

①m1______m2(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
②温度高于T0,COS转化率减小的可能原因为:i有副应发生;ii______;iii______。
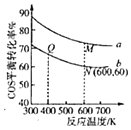
(5)在充有催化剂的恒压密闭容器中进行反应Ⅱ.COS(g)与H2O(g)投料比分别为1:3和1:1,反应物的总物质的量相同时,COS(g)的平衡转化率与温度的关系曲线如图所示:
①M点对应的平衡常数______Q点![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;
;
②N点对应的平衡混合气中COS(g)物质的量分数为______;
③M点和Q点对应的平衡混合气体的总物质的量之比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二胺(H2NCH2CH2NH2),无色液体,电离类似于氨:NH3+H2O![]() NH4++OH-,25℃时,kb1=10-4.07,kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是
NH4++OH-,25℃时,kb1=10-4.07,kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是

A. 曲线Ⅱ代表的微粒符号为H2NCH2CH2NH3+
B. 曲线Ⅰ与曲线II相交点对应pH=6.85
C. 0.1 mol ·L-1H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为c(Cl-)>c(H2NCH2CH2NH3+)>c(H+)>c(OH-)
D. 乙二胺在水溶液中第二步电离的方程式H2NCH2CH2NH3++H2O![]() [H3NCH2CH2NH3]2++OH-
[H3NCH2CH2NH3]2++OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、氧、氟、钙、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1)将乙炔(C2H2)通入[Cu(NH3)2]Cl溶液生成Cu2C2红榇色沉淀。乙炔分子中σ键与π键个数比值为___________,Cu+基态核外电子排布式为___________,[Cu(NH3)2]Cl中化学键类型为___________。
(2)NF3是微电子工业中优良的等离子刻蚀气体。元素第一电离能N___________F(填“>”“<”或“=”),NF3中氮原子的杂化轨道类型为___________,NF3属于___________分子。(填“极性”或“非极性”)
(3)C60可以用作储氢材料。已知金刚石中C-C的键长为154.45pm,C60中C-C的键长为140~145pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?理由是___________。
(4)氮的氧化物和含氧酸在医疗上具有重要的应用。写出与N2O互为等电子体的分子___________(任写一种),酸性HNO3>HNO2,试着从结构上解释其原因___________。
(5)电石(CaC2)是有机合成化学工业的基本原料。CaC2晶体的晶胞结构与NaCl晶体相似(如图所示),但晶体中由于哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中每个Ca2+周围距离最近的C22-的数目为___________,已知CaC2晶体的密度为2.22g·cm-3,该晶胞的体积为___________cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚磷酸(H3PO3)的结构如图 ,具有强还原性的弱酸,可以被银离子氧化为磷酸。
,具有强还原性的弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式__________.
(2)Na2HPO3是____(填“正盐”或“酸式盐”) 正盐
(3)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为______________;
(4)某温度下,0.10molL-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2molL-1,该温度下H3PO3的电离平衡常数K=___________________;(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(5)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)_____c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”,下同);在NaH2PO3溶液中,c(H+)+c(H3PO3)_____c(HPO32-)+c(OH-)
(6)向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中的H3PO3、H2PO3-、HPO32-的物质的量分数a(X)(平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。

以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺环化合物具有抗菌活性,用其制成的药物不易产生抗药性,螺[3,4]辛烷的结构如图,下列有关螺[3,4]辛烷的说法正确的是( )

A. 分子式为C8H16B. 分子中所有碳原子共平面
C. 与2—甲基—3—庚烯互为同分异构体D. 一氯代物有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是

A. 电解过程中,d电极质量增加 B. 电解过程中,氯离子浓度不变
C. a为负极,b为正极 D. a为阳极,b为阴极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com