
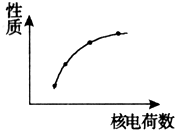
 如图表示第IA族的金属元素的某些性质随核电荷数的变化关系.下列各性质中不符合图示关系的是( )
如图表示第IA族的金属元素的某些性质随核电荷数的变化关系.下列各性质中不符合图示关系的是( )| A. | 金属性 | B. | 阳离子的氧化性 | ||
| C. | 单质与水反应的剧烈程度 | D. | 最高价氧化物对应的水化物的碱性 |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题

| A. | 等物质的量的甲、乙、丙分别与足量钠反应,乙放出气体最多 | |
| B. | 甲、乙、丙均能与Fe3+显色 | |
| C. | 甲和丙互为同分异构体 | |
| D. | 甲、乙、丙苯环上的一溴代物均为4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑤⑦ | C. | ①③④⑥⑧ | D. | ②⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素单质在常温下与水反应不如钠剧烈 | |
| B. | 该元素单质在常温下能与氧气反应 | |
| C. | 该元素最高化合价为+1 | |
| D. | 该元素氢氧化物的水溶液为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4L氧气含分子数为NA个O2 | |
| B. | 1molNa2O2化合物中有2mol阴离子和2mol阳离子 | |
| C. | 2.3g金属钠变为钠离子失去电子数为0.1NA | |
| D. | .常温下,1 L 0.5 mol•L-1 NH4Cl溶液中含有3.01×1023个NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,溶液中由水电离的c(H+)=1.0×10-4mol/L,则该溶液有可能是稀盐酸 | |
| B. | NH4Cl溶液加水稀释后,恢复至原温度,pH和Kw均增大 | |
| C. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| D. | 在Na2S溶液中加入AgCl固体,白色AgCl转变为黑色Ag2S,则溶液中c(S2-)下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com