
【题目】将1.0mol I2 (g)和2.4mcl H2置于某2L密闭容器中,在某一温度下发生反应H2(g)+I2(g)2HI(g)△H<0,并达平衡,12的转化率a(I2)随时间变化如图曲线Ⅱ所示 
(1)若改变反应条件,在某条件下a(I2)的变化如曲 线(I )所示,则该条件可能是:(填序号)
①恒容条件下,升高温度
②恒温条件下,缩小反应容器体积
③恒温条件下,扩大反应容器体积
④恒温、恒容条件下,加入适当催化剂
(2)该温度下此化学反应的化学平衡常数为 .
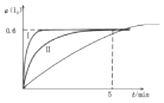
(3)在图基础上画出恒容条件下,降低温度,I2的转化率a(I2)随时间变化的曲线 .
(4)若在原平衡的基础上,保持体系温度不变,再往体系中通入1.4mol I2(g)和0.6mol HI(g),计算再次达到平衡时I2(g)的物质的量.(写出计算过程,已知最后结果保留2位有效数字)
【答案】
(1)②④
(2)2
(3)
(4)解:
H2(g)+ | I2(g) | 2HI(g) | |||
起始量: | 1.8 | 1.8 | 1.8 | ||
变化量: | x | x | 2x | ||
平衡浓度: | 1.8﹣x | 1.8﹣x | 1.8+2x |
所以K= ![]() ,解之得x=0.21,则:再次达到平衡时I2(g)的物质的量1.6mol,
,解之得x=0.21,则:再次达到平衡时I2(g)的物质的量1.6mol,
答:再次达到平衡时I2(g)的物质的量1.6mol.
【解析】解:(1)①恒容条件下,升高温度,反应速率加快,平衡向逆反应方向移动,所以碘的转化率减小,故错误;②恒温条件下,缩小反应容器体积,反应速率加快,达平衡所需时间缩短,但平衡不移动,所以碘的转化率不变,故正确;③恒温条件下,扩大反应容器体积,反应速率减小,达平衡所需时间增长,故错误;④恒温、恒容条件下,加入适当催化剂,反应速率加快,达平衡所需时间缩短,但平衡不移动,故正确;故选②④;
2)
H2(g)+ | I2(g) | 2HI(g) | |||
起始浓度: | 1.2 | 0.5 | 0 | ||
变化浓度: | 0.5×0.6 | 0.5×0.6 | 0.6 | ||
平衡浓度: | 0.9 | 0.2 | 0.6 |
所以K= ![]() =2,
=2,
所以答案是:2;(3)降低温度,达平衡的时间缩智囊,平衡正向移动,I2的转化率增大,所以图象为: 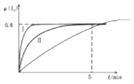 ,所以答案是:
,所以答案是: 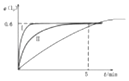 ;
;
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(2015·上海)氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空: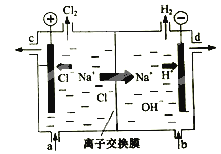
已知: H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7
HClO Ki1=2.95×10-8
H2CO3 Ki1=4.3×10-7 Ki2=5.6×10-11
(1)写出电解饱和食盐水的离子方程式。
(2)离子交换膜的作用为: 、 。
(3)精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、“b”、“c”或“d”)
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2 , 还生成CO2和KHSO4等物质。
写出该反应的化学方程式
(5)室温下,0.1 mol/L NaClO溶液的pH 0.1 mol/L Na2SO3溶液的pH。(选填“大于”、“小于”或“等于”)。
浓度均为0.1 mol/L 的Na2SO3和Na2CO3的混合溶液中,SO32–、CO32–、HSO3–、HCO3– 浓度从大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中,核磁共振氢谱中出现三组峰,且峰面积之比为:2:2:1的是( )
A.CH3CH2CH2OH
B.CH3OCH3
C.CH2=CH﹣CH3
D.一氯苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1mol/L的氨水中加入少量的NH4Cl固体, 溶液的pH(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度(填“增 大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和2H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 , 平衡常数表达式为;若有1mol硝酸铵完全分解,转移的电子数为mol。
(3)由N2O、H2O反应生成N2和NO2的能量变化如图所示,若生成1molN2 , 其△H= kJ/mol。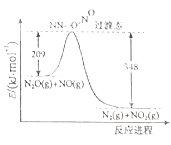
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应(夹持仪器略去)。

(1)A中装有氯化铵和氢氧化钙的混合物,发生反应的化学方程式是___________;
(2)B中加入的是碱石灰,其作用是___________;
(3)实验时C中观察到的现象是___________,发生反应的化学方程式是_____________;
(4)试管D中收集到的物质是___________,向其中滴加酚酞试液,溶液变_____色,原因是___________________(用电离方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)某化学课外研究小组,设计实验探究KI溶液和FeCl3溶液反应存在一定的限度.请完成相关的实验步骤和现象.可选试剂:①0.1molL﹣1KI溶液;②0.1molL﹣1 FeCl3溶液;③FeCl2溶液;④盐酸;⑤KSCN溶液;⑥CCl4 .
实验步骤:①取5mL 0.1molL﹣1 KI溶液,再滴加5~6滴0.1molL﹣1FeCl3溶液
②充分反应后,将溶液分成三份
③取其中一份,滴加试剂CCl4 , 用力振荡一段时间,CCl4层出现紫红色,说明反应生成碘.
④另取一份,滴加试剂(填试剂序号),若现象为 , 该反应有一定的限度.
(2)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题: 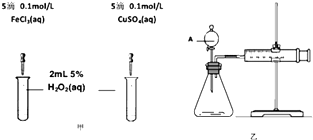
①定性分析:如图甲可通过观察(填现象),定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3溶液更为合理,其理由是 . 写出H2O2在二氧化锰作用下发生反应的化学方程式: .
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.实验中一定需要测量的数据是(填序号).
①收集40mL气体所需要的时间 ②CuSO4溶液和FeCl3溶液的浓度 ③过氧化氢溶液的浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究.在相同温度下,M的物质的量浓度(molL﹣1)随时间(min)变化的有关实验数据见表.下列说法不正确的是( )
时间 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.4 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.4 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Ca2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
A.在0~20 min内,Ⅰ中M的分解速率为0.015 molL﹣1min﹣1
B.水样酸性越强,M的分解速率越快
C.在0~20 min内,Ⅲ中M的分解百分率比Ⅱ大
D.由于Ca2+存在,Ⅳ中M的分解速率比Ⅰ快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物中可能含有:K+、Na+、Clˉ、CO32﹣、SO42﹣等离子,将该固体溶解所得到的溶液进行如下实验:下列说法正确的是( ) 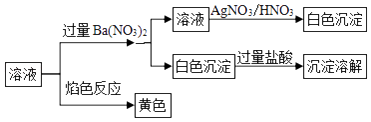
A.该混合物一定是K2CO3和NaCl
B.该混合物可能是Na2CO3和KCl
C.该混合物可能是Na2SO4和Na2CO3
D.该混合物一定是Na2CO3和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色植物是空气天然的“净化器”,研究发现,1亩柳杉每天可以吸收5mol SO2 . 则1亩柳杉每天吸收的SO2的质量为( )
A.320g
B.160g
C.64g
D.32g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com