
| A. | 3S2-+2NO3-+8H+→2NO↑+3S↓+4H2O | |
| B. | S2-+2NO3-+4H+→2NO2↑+S↓+2H2O | |
| C. | Fe3++3NO3-+5H2S+2H+→3NO↑+5S↓+Fe2++6H2O | |
| D. | Fe3++5NO3-+8H2S+4H+→5NO↑+8S↓+Fe2++10H2O |
分析 酸性溶液中,氧化性HNO3>Fe3+,硫化氢不足,硝酸根离子氧化硫化氢;硫化氢足量,则Fe(NO3)3完全反应,以此来解答.
解答 解:酸性溶液中,氧化性HNO3>Fe3+,硫化氢不足,硝酸根离子氧化硫化氢,由电子、电荷守恒可知,离子反应为3H2S+2NO3-+2H+=2NO↑+3S↓+4H2O,
硫化氢足量,则Fe(NO3)3完全反应,由电子、电荷守恒可知,离子反应为Fe3++3NO3-+5H2S+2H+=3NO↑+5S↓+Fe2++6H2O,
故选C.
点评 本题考查离子反应的书写,为高频考点,把握发生的化学反应及电子守恒为解答的关键,侧重氧化还原反应的离子反应考查,注意氧化性的强弱及反应的先后顺序,题目难度中等.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
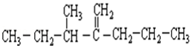 名称为3-甲基-2-丙基-1-戊烯.
名称为3-甲基-2-丙基-1-戊烯.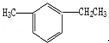 名称为1-甲基-3-乙基苯.
名称为1-甲基-3-乙基苯. 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:
碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | N2$→_{放电}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
| B | NaCl(饱和)$→_{②CO_{2}}^{①NH_{3}}$NaHCO3$\stackrel{△}{→}$Na2CO3 |
| C | Fe$→_{点燃}^{少量Cl_{2}}$FeCl2$\stackrel{Cl_{2}}{→}$FeCl3 |
| D | FeS2$→_{煅烧}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gH2含有的氢原子数目为NA | |
| B. | 常温下,1molCl2与足量NaOH溶液完全反应,转移的电子数为2NA | |
| C. | 常温常压下,11.2L氧气含有的原子数目为NA | |
| D. | 1L1 mol•L-1 KOH溶液中含有的钾离子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com