
| 7.2-0.1��27-0.3��12 |
| 1 |
| 7.2-0.1��27-0.3��12 |
| 1 |
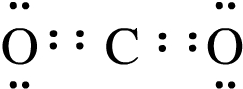 ������Ԫ����ԭ��������������Ԫ�أ������ڱ��е�λ���ǵ�������IIIA�壬
������Ԫ����ԭ��������������Ԫ�أ������ڱ��е�λ���ǵ�������IIIA�壬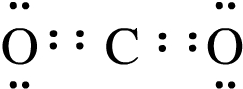 ����������IIIA�壻
����������IIIA�壻 

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| H2O |
| ŨH2SO4 |
| �� |
| Mg |
| ��ˮ���� |
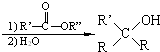
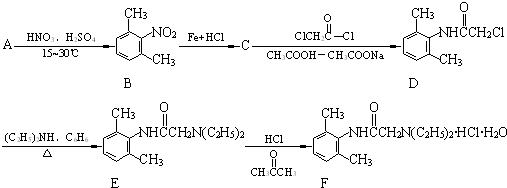
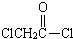 ��������NaOH��Һ���ȳ�ַ�Ӧ�Ļ�ѧ����ʽ��
��������NaOH��Һ���ȳ�ַ�Ӧ�Ļ�ѧ����ʽ��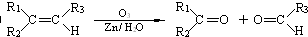
| BBr |
| NaOH��Һ |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Na��Mg��Al�����ʵ���x | x��
|
| �� | �� | ||||
| ����H2����� | �� | �� | V��Na����V��Mg��=V��Al�� | V��Na��=V��Mg��=V��Al�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K2MnO4 |
| B��MnSO4 |
| C��Mn2O3 |
| D��MnO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ӳ�һ���ǽ������ӣ��������ӵ�����һ���������� |
| B����������������ò�һ���γ����ӻ����� |
| C�����ӻ����������ǿ����ʣ���������ˮ |
| D����ij����Ԫ�ص������Ӻ�ij�ǽ���Ԫ����������ɵ�����һ���Ǵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4 |
| B��CO |
| C��C2H4 |
| D��N2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������FeCl3��Һ�����ˮ���Ʊ������������壺Fe3++3H2O=Fe��OH��3��+3H+ |
| B����Ca��HCO3��2�������Ca��OH��2��Ca2++2HCO3-+2OH-=CaCO3��+2H2O+CO32- |
| C����������Һͨ��������CO2��2C6H5O-+CO2+H2O��2C6H5OH+CO32- |
| D����ȩ��������Һ��Ӧ��CH3CHO+2Ag��NH3��2++2OH-��CH3COO-+NH4++2Ag��+3NH3+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com