
【题目】(1)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:_____。

(2)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)═2H2O(l)。请回答下列问题:
①该反应的生成物能量总和____(填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量____(填“大于”、“小于”或“等于”)572kJ。
(3)已知拆开1molN﹣N键、1molN﹣H键、1molN≡N键、O=O键需要的能量分别是3akJ、2.5akJ、8akJ、4akJ,完全燃烧1mol火箭燃料肼(N2H4)生成氮气和水蒸气放出能量为5akJ,则1molH2O(g)完全断键时共吸收____kJ的能量。
(4)已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,反应物的总键能_____(填“大于”、“小于”或“等于”)生成物的总键能。

【答案】E2>E3>E1 小于 小于 4a 大于
【解析】
(1)化学反应的本质即是旧键的断裂和新键的形成过程,旧键断裂吸收能量,新键形成放出能量,这是化学反应中能量变化的主要原因,据此进行分析。
(2)①由反应热ΔH=生成物的总能量-反应物的总能量进行判断。
②同一物质状态由气→液→固变化时,会放热,反之,会吸热。据此进行分析。
(3)由反应热ΔH=反应物的键能总和-生成物的键能总和进行计算判断。
(4)分析题给能量变化图,根据放热反应中其反应物具有的总能量大于生成物具有的总能量,吸热反应中反应物具有的总能量小于生成物具有的总能量,进行判断。
(1)E1~E2的过程,为旧化学键断裂而吸收能量的过程,故E1<E2,E2~E3的过程,为新化学键形成而放出能量的过程,则:E2>E3,根据题给信息,反应为吸热反应,则有:E1<E3,故E1、E2、E3的大小关系为:E2>E3>E1,故答案为:E2>E3>E1;
(2)①反应放出热量,说明反应物具有的能量总和大于生成物具有的能量总和,故答案为:小于;
②因同一物质状态由气→液→固变化时,会放热,即同一物质气态时具有的能量高于该物质液态时所具有的能量,则2mol氢气燃烧生成液态水时放出572kJ的热量,若生成水蒸气,则放出的能量小于572kJ。答案为:小于;
(3)根据题意可知肼燃烧的热化学反应方程式为:N2H4+O2=2H2O+N2 ΔH=-5akJ/mol。根据反应热ΔH=反应物的总键能之和-生成物的总键能之和,设1molH-O键断裂时需要能量为x,有:![]() ,解得:
,解得:![]() ,则1mol H2O(g)完全断键时吸收的能量为:4akJ。故答案为:4a。
,则1mol H2O(g)完全断键时吸收的能量为:4akJ。故答案为:4a。
(4)分析题给能量变化图可知,反应物所具有的能量低,生成物具有的能量高,则总反应为吸热反应,则反应物的总键能大于生成物的总键能,答案为:大于。
物质 | CO2 (C=O) | CH4 (C-H) | P4 (P-P) | SiO2 (Si-O) | 石墨 (C-C) | 金刚石 (C-C) | S8 (S-S) | Si (Si-Si) |
键数 | 2 | 4 | 6 | 4 | 1.5 | 2 | 8 | 2 |


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(s)ΔH >0,若0~15 s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是( )
H2(g)+I2(s)ΔH >0,若0~15 s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是( )
A. 0~15 s内用I2表示的平均反应速率为v(I2)=0.001 mol·L-1·s-1
B. c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需的反应时间小于10 s
C. 升高温度正反应速率加快,逆反应速率也加快
D. 减小反应体系的体积,正逆反应速率增大程度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定物质的量浓度的NaOH溶液100 mL,向其中通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1mol/L的HCl溶液,产生的CO2气体体积 (标准状况)与所加HCl溶液的体积之间关系如图所示,请回答:

(1)A溶液中的溶质_________。(用化学式表示)
(2)通入的CO2的体积(标准状况)为_______ mL。
(3)NaOH溶液的物质的量浓度_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为几种晶体或晶胞的示意图:


请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是____。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:___。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___(填“大于”或“小于”)MgO晶体,原因是____。
(4)每个Cu晶胞中实际占有___个Cu原子,CaCl2晶体中Ca2+的配位数为__。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式能用来解释相应实验现象的是
实验现象 | 离子方程式 | |
A | 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 |
|
B | 向沸水中滴加饱和氯化铁溶液得到红褐色液体 |
|
C | 二氧化硫使酸性高锰酸钾溶液褪色 |
|
D | 氧化亚铁溶于稀硝酸 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应CO(g)+H2O(g)![]() CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
A. 加入催化剂,改变了反应的途径,反应的△H也随之改变
B. 改变压强,平衡不发生移动,反应放出的热量不变
C. 升高温度,反应速率加快,反应放出的热量不变
D. 若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化剂、漂白剂,主要用于亚麻、纸浆等漂白。NaClO2在溶液中可生成ClO2、HClO2、ClO2-、Cl-等含氯微粒,经测定,25 ℃时各组分含量随pH变化情况如图所示(部分没有画出)。则下列分析不正确的是

A. 亚氯酸钠在碱性条件下较稳定
B. 25 ℃时,HClO2的电离平衡常数Ka=10-6
C. 25 ℃,pH=3时NaClO2溶液中c(Na+)+c(H+)=c(ClO2-)+c(OH-)
D. 等浓度的HClO2溶液和NaClO2溶液等体积混合的溶液中(pH<7):c(ClO2-)>c(Na+)>c(HClO2)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
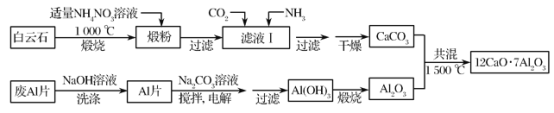
(1)煅粉主要含MgO和________,用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,若溶液Ⅰ中c(Mg2+)小于5×10-6mol·L-1,则滤液pH大于________[Mg(OH)2的Ksp=5×10-12];该工艺中不能用(NH4)2SO4代替NH4NO3,原因是______________。
(2)滤液Ⅰ中的阴离子有________(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为_________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式________。
(5)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应aM(g)+bN(g)![]() cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如下图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。下列说法正确的是
cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如下图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。下列说法正确的是

A. 同温同压同z时,加入催化剂,平衡时Q的体积分数增加
B. 同压同z时,升高温度,平衡时Q的体积分数增加
C. 同温同z时,增加压强,平衡时Q的体积分数增加
D. 同温同压时,增加z,平衡时Q的体积分数减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com