
| A. | 一定条件下,气体体积大小取决于气体分子的大小 | |
| B. | 一定条件下,气体体积大小取决于其物质的量的多少 | |
| C. | 1mol任何气体所占的体积为22.4L,称为气体摩尔体积 | |
| D. | 体积不相等的两种气体所含的分子数也一定不相等 |
分析 A.一定条件下,气体体积取决于气体分子数;
B.一定条件下气体摩尔体积相同,根据V=nVm可知,气体体积与物质的量成正比;
C.标准状况下,1mol气体体积约为22.4L,否则不一定满足该关系;
D.相同条件下,体积不同的气体具有不同分子数,没有告诉温度和压强,体积不相等的两种气体所含的分子数可能相等.
解答 解:A.气体体积的大小主要取决于构成气体的分子数目的多少,而与分子大小无关,故A错误;
B.一定条件下,气体摩尔体积相同,根据V=nVm可知气体体积大小取决于其物质的量的多少,故B正确;
C.单位物质的量的气体占有的体积称为气体摩尔体积,标准状况下1mol气体体积约为22.4L,否则不一定满足,故C错误;
D.由于温度和压强影响气体体积,所以体积不相等的两种气体所含的分子数可能相等,故D错误;
故选B.
点评 本题考查了物质的量的应用,题目难度不大,明确标准状况下气体摩尔体积与气体摩尔体积的关系为解答关键,注意掌握物质的量与其它物理量之间的关系,试题培养了学生的化学计算能力.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 适量施用化学肥料和农药 | |
| B. | 大量开采地下水,以满足社会对水的需求 | |
| C. | 减少直至不使用对大气臭氧层起破坏作用的氟氯烃 | |
| D. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
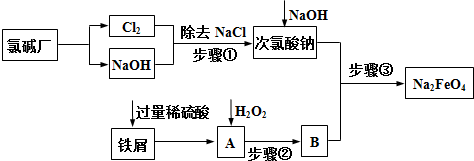
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体是很稳定的分散系,比溶液还稳定 | |
| B. | 胶体能发生丁达尔现象 | |
| C. | 胶体的分散质不能透过滤纸 | |
| D. | 胶体不稳定,静止后容易产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同一弱电解质溶液,温度不同时,导电能力相同 | |
| B. | 强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强 | |
| C. | 强电解质在水溶液中的电离过程是不可逆的 | |
| D. | 易溶于水的电解质一定是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
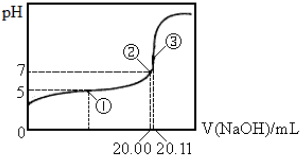
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com