
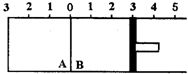
 如图所示,温度不变时某容器分隔A、B两部分,A容积固定不变,B有可移动的活塞,现有A中充入2molSO2和1molO2,在B中充入2molSO3(g),在体积相同的条件下发生可逆反应:2SO2+O2?2SO3.根据下列要求填写空白:
如图所示,温度不变时某容器分隔A、B两部分,A容积固定不变,B有可移动的活塞,现有A中充入2molSO2和1molO2,在B中充入2molSO3(g),在体积相同的条件下发生可逆反应:2SO2+O2?2SO3.根据下列要求填写空白:分析 (1)A中充入2molSO2和1molO2,在B中充入2molSO3(g)建立的平衡是等效的;
(2)如果活塞可自由移动,当容器A.B中均达到平衡状态,根据气体的密度等于质量和物质的量的比值来判断;随反应进行,气体的物质的量减小,所以恒容容器内部压强减下,恒压相当于在恒容的基础上加压,据此回答.
解答 解:(1)A中充入2molSO2和1molO2,在B中充入2molSO3(g)建立的平衡是等效的,若固定活塞位置在右侧的3处不动,达到平衡时,PA=PB,
故答案为:等于;
(2)随反应进行,气体的物质的量减小,所以恒容容器内部压强减下,恒压相当于在恒容的基础上加压.如果活塞可自由移动,当容器A.B中均达到平衡状态,气体的密度等于质量和物质的量的比值,此时A中气体的密度会大于B中气体的密度,此时SO3的百分含量的关系是A>B,
故答案为:大于;大于.
点评 本题考查了化学平衡的计算,主要考查等效平衡及其判断的知识,题目难度中等,明确等效平衡的含义、正确判断等效平衡为解答关键,注意掌握化学平衡及其影响因素,试题培养了学生的分析、理解能力及灵活应用所学知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
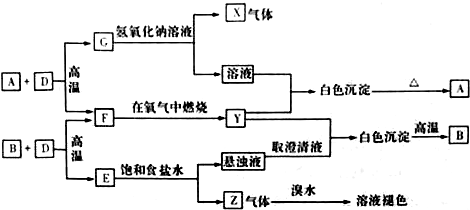
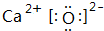 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | |
| ① | NaOH溶液 | Al | Fe2O3 |
| ② | KOH溶液 | Br2 | Na2SO3溶液 |
| ③ | Na2CO3 | SiO2 | H2O |
| ④ | HCl | NaHCO3 | NaOH |
| A. | 只有①③④ | B. | 只有①②④ | C. | 只有①②③ | D. | ①②③④皆可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | NaOH溶液与醋酸溶液反应后所得的pH大于7的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )
常温下,向10mL 0.1mol•L-1的CH3COOH溶液中逐滴加入0.1mol•L-1 NaOH溶液,所得滴定曲线如图所示.下列说法一定正确的是( )| A. | A点的pH为1 | |
| B. | B点时:2c(H+)+c(CH3COOH)═2c(OH-)+c(CH3COO-) | |
| C. | 在A→B之间:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | C点时:c(H+)+c(Na+)═c(OH-)+c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com