
【题目】聚乙烯醇缩甲醛有热塑性,耐磨,可以制造高强度漆包线。由A制备聚乙烯醇缩甲醛等的合成路线(部分反应条件略去)如下所示:
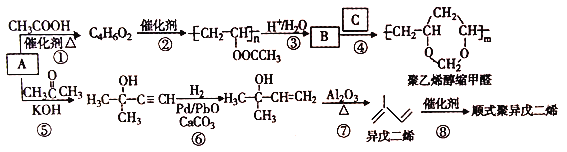
回答下列问题:
(1)A的结构简式是________,B含有的官能团名称是________;①的反应类型是______,⑦的反应类型是_________。
(2)B和C的结构简式分别为_______、_______。
(3)异戊二烯分子中最多有_____个原子共平面,顺式聚异戊二烯的结构简式为_______;写出与A具有相同官能团的异成二烯的所有同分异构体_______ (填结构简式)。
(4)参照异戊二烯的上述合成路线,设计一条由A和乙醛为起始原料制备1,3-丁二烯的合成路线_______。
【答案】 CH≡CH 羟基 加成反应 ;消去反应 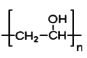 HCHO 11
HCHO 11 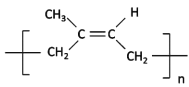 HC≡C-CH2CH2CH3 CH3C≡C-CH2CH3
HC≡C-CH2CH2CH3 CH3C≡C-CH2CH3 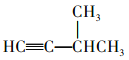
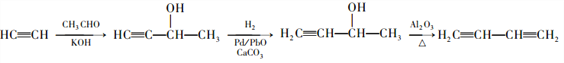
【解析】(1)根据A与醋酸反应、A与丙酮反应的特征分析,A为含有2个碳原子的不饱和烃,A的分子式是![]() ,可知A为乙炔;根据B反应生成聚合物
,可知A为乙炔;根据B反应生成聚合物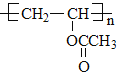 可知B的结构简式为
可知B的结构简式为![]() ,故B中含有的官能团为碳碳双键和酯基;
,故B中含有的官能团为碳碳双键和酯基;![]() 和
和![]() 反应生成
反应生成![]() ,碳碳三键中的一条键断开,可知该反应为加成反应;
,碳碳三键中的一条键断开,可知该反应为加成反应;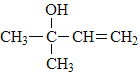 反应生成
反应生成![]() ,失去了一分子
,失去了一分子![]() ,生成碳碳双键,故该反应为消去反应;正确答案:CH≡CH ; 羟基; 加成反应;消去反应 。
,生成碳碳双键,故该反应为消去反应;正确答案:CH≡CH ; 羟基; 加成反应;消去反应 。
(2)
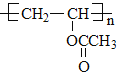 酸性条件下酯基发生水解生成
酸性条件下酯基发生水解生成 ,因此B的结构简式为
,因此B的结构简式为 ;有机物B与C发生羟醛缩合反应生成
;有机物B与C发生羟醛缩合反应生成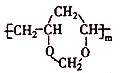 ,所以有机物C为HCHO; 正确答案:
,所以有机物C为HCHO; 正确答案: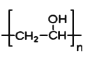 ; HCHO。
; HCHO。
(4)![]() 中甲基为四面体结构,最多2个原子共平面,当两个碳碳双键位于同一平面时,共面原子数最多,因此最多有11个原子共平面;顺式聚异戊二烯的结构简式为
中甲基为四面体结构,最多2个原子共平面,当两个碳碳双键位于同一平面时,共面原子数最多,因此最多有11个原子共平面;顺式聚异戊二烯的结构简式为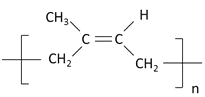 ; A的官能团为碳碳三键,因此该有机物满足分子式为
; A的官能团为碳碳三键,因此该有机物满足分子式为![]() ,含有碳碳三键,这样的同分异构体有三种:
,含有碳碳三键,这样的同分异构体有三种:![]() 、
、![]() 、
、![]() ;正确答案:11 ;
;正确答案:11 ; 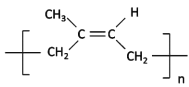 ; HC≡C-CH2CH2CH3 、CH3C≡C-CH2CH3
; HC≡C-CH2CH2CH3 、CH3C≡C-CH2CH3 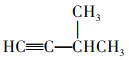 。
。
4)类比反应⑤可知乙炔和乙醛反应生成![]() ,由⑥可知碳碳三键发生部分加成反应生成
,由⑥可知碳碳三键发生部分加成反应生成![]() ,再类比反应⑦可知羟基发生消去反应生成碳碳双键,得到1,3-丁二烯,合成路线如下:
,再类比反应⑦可知羟基发生消去反应生成碳碳双键,得到1,3-丁二烯,合成路线如下:
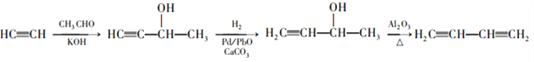 ;
;
正确答案: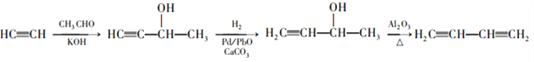 。
。


科目:高中化学 来源: 题型:
【题目】最近全球多个国家爆发大规模流感,中药良好的预防和治疗作用再次进入科学家的视野。食用香料肉桂具有良好的预防作用,其有效成分之一肉桂酸结构简式如图所示。下列说法不正确的是
![]()
A. 肉桂酸的化学式为C9H8O2
B. 肉桂酸能发生加成反应、取代反应
C. 肉桂酸的结构中含有4个碳碳双键
D. 肉桂酸能使溴水、酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,将2molCO与5molH2的混合气体充入容积为2L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
(1)经过5min后,反应达到平衡,此时转移电子6mol。该反应的平衡常数为_______。V(H2)=_____mol/(L·min)。若保持体积不变,再充入2mulCO和1.5mol CH3OH,此时v(正)___ v(逆)(填“>”“<”或“=”)。
(2)在其他条件不变的情况下,再增加2molCO与5molH2,达到新平衡时,CO的转化率____(填“增大”“减小”或“不变”)。
(3)下列不能说明该反应已达到平衡状态的是__________
a.CH3OH的质量不变 b.混合气体的平均相对分子质量不再改变
c.V逆(CO)=2V正(H2) d.混合气体的密度不再发生改变
(4)在一定压强下,容积为VL的容器充入amolCO与2amolH2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
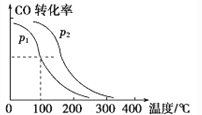
则p1_____p2(填“大于”“小于”或“等于”,下同),△H_____0。该反应在_______(填“高温”或“低温”)下能自发进行。
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是_____。
a.及时分离除CH3OH气体 b.适当升高温度
c.增大H2的浓度 d.选择高效催化剂
(6)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是_______。
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.有效碰撞理论可指导怎样提高原料的转化率
c.勒夏特列原理可指导怎样使用有限原料多出产品
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化亚铁易被氧化,制取过程要隔绝空气。现用铁屑、稀硫酸、氢氧化钠溶液制备氢氧化亚铁并观察其颜色,改进装置如下:
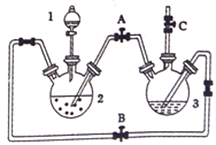
(1)稀硫酸应放在_____________(填写仪器名称)中。
(2)本实验通过关闭开关________、打开开关_________,将仪器中的空气排尽后,后续实验就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由___________________。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备莫尔盐晶体[(NH4)2SO4·FeSO4·6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是___________
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用30%的乙醇溶液洗 d.用90%的乙醇溶液洗
②为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液。每次取待测液20.00mL,用浓度为bmol/L的酸性KMnO4溶液滴定,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗酸性高锰酸钾溶液体积/mL | 20.02 | 19.98 | 20.52 |
滴定过程中发生反应的离子方程式为______________。滴定终点的现象是__________________________。通过实验数据计算的该产品纯度为_____________(用字母a、b表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=1。反应前CO物质的量为1mol,平衡后CO物质的量为0.5mol。下列说法正确的是( )
COS(g)+H2(g) K=1。反应前CO物质的量为1mol,平衡后CO物质的量为0.5mol。下列说法正确的是( )
A. 羰基硫的电子式为: :![]() :
:![]() :
:![]() :
:
B. 通入CO后,正反应速率逐渐增大
C. 再加入0.1molH2S和0.1molH2,平衡不移动
D. 反应前H2S物质的量为0.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A. 4Fe(OH)2+2H2O+O2===4Fe(OH)3↓
B. 2Fe+2H2O+O2===2Fe(OH)2↓
C. 2H2O+O2+4e-===4OH-
D. Fe-3e-===Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,回答有关问题:
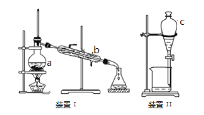
(1)写出装置I中有关仪器的名称:a ________________,b__________________,该装置分离混合物的原理是根据混合物各组分______________不同进行分离的。
(2)装置II中仪器C 的名称为_______________,使用C前必需进行的操作是 _______________为使C中液体顺利流下,打开活塞前应进行的操作是 _________________________。
(3)下面是用36.5%的浓盐酸(ρ=1.19g/cm3)配制250mL 0.5mol/L的稀盐酸 的操作,请按要求填空:
①配制上述溶液所需的玻璃仪器除玻璃棒、量筒、烧杯,还有 _____________________,需要量取浓盐酸的体积为 ____________mL。
②下列操作中,会造成所配溶液浓度偏低的是______(填字母)。
a.定容时,俯视刻度线 b.没有洗涤烧杯和玻璃棒
c.洗涤后的容量瓶中残留少量蒸馏水。d.量筒量取盐酸前没有用浓盐酸润洗。
③经测定,所配溶液的浓度偏小,如果忽略实验过程产生的误差,可能的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为__________。氧元素与氟元素能形成OF2分子,氧原子轨道杂化类型__________。
(2)根据等电子体原理,NO2+的空间构型是__________;1 molN O2+中含有的π键数目为__________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。基态铬原子外围电子排布式为__________。
(4)下列物质的分子与O3分子的结构最相似的是__________。
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子?__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com