
| 1000ρw |
| M |
| n |
| V |
| 1 |
| 5 |
| 1000×1.84g/cm3×98% |
| 98g/mol |
| 1 |
| 5 |
| 1 |
| 5 |


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
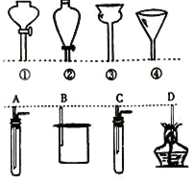 ①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与
①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在晶体中只要有阳离子就一定有阴离子 |
| B、加热至沸腾蒸发水分时,溶液的浓度一定增大 |
| C、一个原子或单核离子,最外层有8个电子时,一定达到了稳定结构 |
| D、水的分子量不到空气平均分子量的2/3,如果水分子间没有特殊的作用力,地球上就不会有液态水 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝是地壳中含量最多的金属元素 |
| B、铝的抗腐蚀性能好,原因是铝表面的氧化膜可以阻止铝与空气中的氧气接触 |
| C、铝是一种活泼的金属,在化学反应中常作还原剂 |
| D、铝制餐具能用于蒸煮,或长时间存放碱性食物,但不适宜存放酸性食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行蒸发操作时,应将混合物中的水分完全蒸干后,才能停止加热 |
| B、进行蒸馏操作时,蒸馏烧瓶中应加入几粒沸石 |
| C、进行分液操作时,分液漏斗中下层液体先从下口放出,上层液体后从下口放出 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉、油脂、蛋白质都能水解,且水解产物各不相同 |
| B、从煤的干馏产物中可以获得焦炉气、粗氨水、煤焦油、焦炭等重要的化工原料 |
| C、石油催化裂化的主要目的是提高芳香烃的产量 |
| D、核酸是一类含磷的生物高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com