
 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行了有关实验:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行了有关实验:分析 (1)依据实验产生的气体是二氧化硫,二氧化硫密度比与空气大,确定收集实验中产生的气体的装置中导气管的位置;
(2)①铜与浓硫酸在加热条件下生成硫酸铜、二氧化硫和水;
②随着反应的进行,浓硫酸逐渐成为稀硫酸,而铜与稀硫酸不反应;
③根据反应后必有硫酸铜产生,所以要证明反应结束后的烧瓶中确有余酸,只有证明氢离子即可;
(3)①A、碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大;
B、高锰酸钾溶液中含有硫酸,与氯化钡反应生成沉淀增大;
C、二氧化硫在水中以1:40溶解,收集二氧化硫体积减少;
D、亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大;
(4)可利用剩余的稀硫酸与锌反应放出氢气,通过氢气的量计算剩余硫酸的物质的量浓度;
解答 解:(1)铜跟浓硫酸反应生成了二氧化硫气体,二氧化硫密度比与空气大,可以用向上排气法收集,所以装置中的导气管应长进短出,装置图为:
故答案为:B装置中导气管长进短出;
(2)①铜与浓硫酸在加热条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O;
②铜与浓硫酸在加热条件下可以发生反应,而铜与稀硫酸不反应,随着反应的进行,硫酸浓度浓度降低,当浓硫酸逐渐成为稀硫酸时反应停止;
故答案为:随着反应进行,硫酸被消耗,浓硫酸变成稀硫酸,稀硫酸和铜不反应;
③根据反应后必有硫酸铜产生,所以要证明反应结束后的烧瓶中确有余酸,只有证明氢离子,
A、铁粉与氢离子反应产生气泡,故A正确;
B、BaCl2溶液只能与硫酸根产生沉淀,故B错误;
C、银粉不反应,无现象,故C错误;
D、Na2CO3溶液与氢离子反应产生气泡,故D正确;
故选:AD;
(3)A、碱石灰除吸收二氧化硫外还能吸收水,测得二氧化硫质量增大,导致余酸的物质的量浓度偏低,故A错误;
B、用排饱和NaHSO3溶液的方法测出装置A产生气体的体积,二氧化硫在饱和NaHSO3溶液中的溶解度降低,可以用排水量气方法进行二氧化硫的气体体积测定,故B正确;
C、二氧化硫在水中以1:40溶解,收集二氧化硫体积减少,导致余酸的物质的量浓度偏高,故C错误;
D、亚硫酸钡在空气中烘干及称重过程中部分被氧化生成硫酸钡,产生固体质量增大,导致余酸的物质的量浓度偏低;
故选:B;
(4)Zn和稀硫酸反应生成氢气,因此可向反应后溶液中加入足量的锌粒,收集并测定氢气的体积,通过氢气量计算剩余硫酸的物质的量浓度;
故答案为:①取反应后溶液,向其中加入足量锌;②收集并测定氢气的体积;③通过氢气量计算剩余硫酸的物质的量浓度.
点评 本题考查了铜跟浓硫酸的反应情况,涉及反应产物的验证、测定方法的设定和判断,关键是产物中的二氧化硫的性质应用和含量测定是解题的难点,难度较大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 该溶液的pH=4 | |
| B. | 适当升高温度,溶液的pH不变 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 由HX电离出的c(H+)约为水电离出的c(OH-)的106倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 序号 | 实验步骤 | 预期现象 | 结论 |
| 1 | |||
| 2 | 锥形瓶中液体含大量Br- | ||
| 3 | 锥形瓶中液体含大量H+ |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
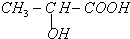 ,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. (用相关的化学用语作答).
(用相关的化学用语作答).| 元素 | Mn | Fe |
| 电离能 | ||
| (kJ•mol-1) | ||
| I1 | 717 | 759 |
| I2 | 1 509 | 1561 |
| I3 | 3 248 | 2 957 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 鸡蛋白溶液中分别滴入饱和硫酸铵和醋酸铅溶液 | 均有固体析出 | 均发生变性 |
| B | 溴水中分别加入苯酚和环己烯 | 溴水均褪色 | 均发生加成反应 |
| C | 某无色气体通入溴水中 | 溴水褪色 | 该气体一定是C2H4 |
| D | 适量水玻璃加入稀盐酸中, 振荡得透明溶液,用激光笔照射 | 有丁达尔效应 | 有硅酸胶体生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2OH+HBr$→_{H+}^{△}$CH3CH2CH2Br+H2O | |
| B. |  +NaHCO3→ +NaHCO3→ +H2CO3 +H2CO3 | |
| C. |  +CO2+H2O→ +CO2+H2O→ +NaHCO3 +NaHCO3 | |
| D. |  +3Br2→ +3Br2→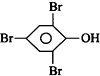 ↓+3HBr ↓+3HBr |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com