
 肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.H分子中含有1个-CH3,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).试回答下列问题.
肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.H分子中含有1个-CH3,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).试回答下列问题.
 ,分子式为C10H10O2,不饱和度为
,分子式为C10H10O2,不饱和度为| 2×10+2-10 |
| 2 |
 ;
;| 2×9+2-10 |
| 2 |
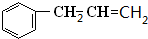 ,A与溴发生加成反应生成B为
,A与溴发生加成反应生成B为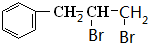 ,B发生水解反应生成C为
,B发生水解反应生成C为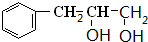 ,C发生催化氧化生成D为
,C发生催化氧化生成D为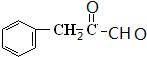 ,D与银氨溶液反应、酸化得到E为
,D与银氨溶液反应、酸化得到E为 ,由F的分子式可知应为
,由F的分子式可知应为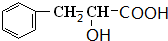 ,F可发生缩聚反应生成I,I为
,F可发生缩聚反应生成I,I为 ,F发生消去反应生成G,为
,F发生消去反应生成G,为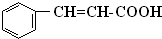 ,H为肉桂酸甲酯;
,H为肉桂酸甲酯; ,分子式为C10H10O2,不饱和度为
,分子式为C10H10O2,不饱和度为| 2×10+2-10 |
| 2 |
 ,
, ;
;| 2×9+2-10 |
| 2 |
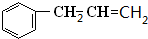 ,A与溴发生加成反应生成B为
,A与溴发生加成反应生成B为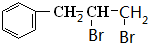 ,B发生水解反应生成C为
,B发生水解反应生成C为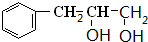 ,C发生催化氧化生成D为
,C发生催化氧化生成D为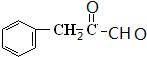 ,D与银氨溶液反应、酸化得到E为
,D与银氨溶液反应、酸化得到E为 ,由F的分子式可知应为
,由F的分子式可知应为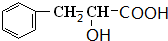 ,F可发生缩聚反应生成I,I为
,F可发生缩聚反应生成I,I为 ,F发生消去反应生成G,为
,F发生消去反应生成G,为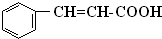 ,H为肉桂酸甲酯;
,H为肉桂酸甲酯;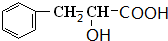 ,化合物F中的官能团有羧基和羟基,
,化合物F中的官能团有羧基和羟基,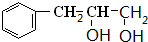 ,C发生催化氧化生成D为
,C发生催化氧化生成D为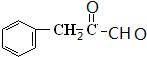 ,反应的方程式为
,反应的方程式为 ,F发生消去反应生成G,F→G的反应方程式为
,F发生消去反应生成G,F→G的反应方程式为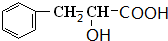
| 浓H2SO4 |
| △ |
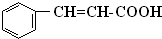 +H2O,
+H2O, ;
;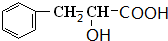
| 浓H2SO4 |
| △ |
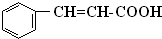 +H2O;
+H2O; ,
, .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 | 淀粉溶液的 用量/mL | 温度/℃ | 酸 | 加酸后溶液中 c(H+)/mol?L-1 | 蓝色褪去所需的 时间/min |
| 1 | 30 | 50 | 盐酸 | 0.01 | 40 |
| 2 | 30 | T1 | 盐酸 | 0.05 | 20 |
| 3 | 30 | T2 | 盐酸 | 0.10 | 8 |
| 4 | 30 | T3 | 硫酸 | 0.05 | 12 |
| 5 | 30 | T4 | 醋酸 | a | 15 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( ) | A、①②③ | B、③④⑤ |
| C、④⑤⑥ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 | |
| 2 | ① | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com