
���淴ӦA(g)+B C(g)+D��A��C��Ϊ��ɫ���壬B��D�ľۼ�״̬δ֪������Ӧ��
C(g)+D��A��C��Ϊ��ɫ���壬B��D�ľۼ�״̬δ֪������Ӧ��
��ƽ��ʱ��������������ȷ����
A�������ֺ��ݣ�����C�������������ɫ�����˵��B������ɫ������
B���������¶ȣ�����C�����ʵ������٣���˵������ӦΪ���ȷ�Ӧ
C����ѹ��������ƽ�ⲻ�ƶ�����˵��B��Dһ����������
D�����ֺ��ݣ�����ƽ����������A��ʹB��ת��������A��ת���ʼ���
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������Һ�������ͺ��Ȼ�����Һ ��39�����Ҵ���Һ ���Ȼ��ƺ͵������ˮ��Һ���������ϸ����Һ����ȷ���������� �� ��
A . ��Һ��������ȡ B. ��ȡ������Һ
C . ��Һ����ȡ������ D. ������ȡ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
˫�ǻ���̼������ҽ���ϳ��õ�һ����������仯ѧʽ��NaAl(OH)2CO3�����ڸ����ʵ�˵����ȷ���ǣ� ��
A.���������������������� B.��������Al(OH)3��Na2CO3�Ļ����
C.1 mol NaAl(OH)2CO3��������3 mol H+ D.��ҩ�����ʺ���θ�����߷���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��ѧ��ӦA2(g) + B2(g) �� 2AB(g)�������仯��ͼ��ʾ��
�ж�������������ȷ����
A��ÿ����2����AB����b kJ����
B���÷�Ӧ�ȡ�H=+��a-b��kJ��mol-1
C���÷�Ӧ�з�Ӧ��������������������������
D������1molA��A��1molB��B�����ų�a kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������巴Ӧ���е�;���ء�����A��һ�������¿ɷ���һϵ��ת��������ͼ�ж�����
������巴Ӧ���е�;���ء�����A��һ�������¿ɷ���һϵ��ת��������ͼ�ж�����
��ϵ�������
A��A��F����H = - ��H 6
B����H1+��H 2+��H 3+��H 4+��H 5+��H 6=1
C��C��F��|��H| = |��H 1+��H 2+��H 6 |
D����H 1+��H 2+��H 3 = -��H 4-��H5-��H 6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£�������X������Y��0.16 mol����10L�����ܱ������У�������ӦX(g)+Y(g) 2Z(g) ��H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
2Z(g) ��H<0��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A����Ӧǰ2min��ƽ������v(Z)=2.0��10-3 mol��L-1��min-1
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��)>v(��)
C�����¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
D�������������䣬�ٳ���0.2 mol Z��ƽ��ʱX�����������ԭƽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������֯��WHO����ClO2��ΪA1����Ч��ȫ���������������ʳƷ���ʡ�����ˮ���������й㷺��Ӧ�á�ClO2����
A. �� B. �� C. �Ȼ��� D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij���������CH4��CO��ɣ��ڱ�״���²���ܶ�Ϊ1g/L����û��������CH4��CO�����ʵ���֮��Ϊ
A��11 B 12 C�� 23 D��78
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijCuSO4��Fe2(SO4)3��H2SO4�Ļ����Һ100 mL����֪��Һ�������ӵ�Ũ����ͬ(������ˮ��)����SO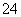 �����ʵ���Ũ��Ϊ6 mol·L��1�������Һ������ܽ�����۵�����Ϊ(����)
�����ʵ���Ũ��Ϊ6 mol·L��1�������Һ������ܽ�����۵�����Ϊ(����)
A��5.6 g B��11.2 g C��22.4 g D��33.6 g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com