
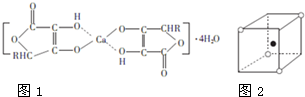
 钙的化合物在共农业生产和生活中有广泛的应用.
钙的化合物在共农业生产和生活中有广泛的应用.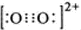 ,在1个O22+含有2个π键,故1 mol O22+中,含有2NA个 π键,故答案为:
,在1个O22+含有2个π键,故1 mol O22+中,含有2NA个 π键,故答案为: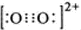 ;2NA;
;2NA;| 1 |
| 8 |
| 1 |
| 2 |
| x | ||
|
19+40×
| ||
| NA |
19+40×
| ||
| NA |
| x | ||
|
| 2 |
| 3 |
| ||
| 2 |
| 3 |
| ||


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 钥匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.3℃ | |
| ② | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验步骤编号 | 实验操作 | 预期现象和结论 |
| ① | 待硬质玻管冷却到室温后,用药匙取少量白色固体于试管中. | / |
| ② | 向①的试管中加入 | |
| ③ | ||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

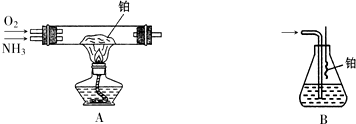
查看答案和解析>>
科目:高中化学 来源: 题型:
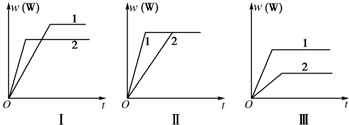
| A、图Ⅰ可能是不同压强对反应的影响,且p1>p2,a+b<n |
| B、图Ⅱ可能是不同压强对反应的影响,且p1>p2,n<a+b |
| C、图Ⅱ可能是在同温同压下不同催化剂对反应的影响,且1使用的催化剂效果好 |
| D、图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
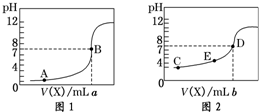
| A、图2是滴定盐酸的曲线 |
| B、a与b的关系是:a<b |
| C、E点对应离子浓度由大到小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、这两次滴定都可以用甲基橙作为指示剂且颜色变化为红变橙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com