
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
【答案】(1)蒸馏烧瓶 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
(2)溶液由紫红色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性
![]()
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH
【解析】试题分析:(1)根据仪器的特征,该仪器是蒸馏烧瓶;亚硫酸钠和浓硫酸反应生成硫酸钠、SO2和水,化学方程式为Na2SO3+H2SO4(浓)= Na2SO4+SO2↑+H2O。
(2)酸性高锰酸钾有强氧化性,二氧化硫中硫元素是中间价态,有还原性,所以二氧化硫能被酸性高 锰酸钾溶液氧化而褪色,同时说明二氧化硫有还原性,SO2的氧化性能将S2-氧化成S,则实验过程中,装置B、C中发生的现象分别是溶液由紫红色变为无色、无色溶液中出现黄色浑浊,这些现象分别说明SO2具有的性质是还原性和氧化性;装置B中发生反应的离子方程式为5SO2+2MnO4-+2H2O =2Mn2++5SO42-+4H+。
(3)二氧化硫具有漂白性,能使品红溶液褪色,但加热褪色后的品红溶液,溶液的颜色能复原,所以探究SO2与品红作用的可逆性的实验操作及现象是品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢复为红色。
(4)该实验的尾气是SO2,SO2用NaOH溶液吸收。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】下列科学家及对应的成就正确的是( )
A. 道尔顿—提出原子学说B. 阿伏伽德罗—提出元素概念
C. 门捷列夫—提出燃烧的氧化说D. 波义尔—提出分子学说
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷(Clopidogrel)是一种用于抑制血小板聚集的药物.以A为原料合成氯吡格雷的路线如下:
已知:R﹣CHO ![]()
![]() ,R﹣CN
,R﹣CN ![]() RCOOH
RCOOH
请回答下列问题:
(1)A中含氧官能团的名称为 , C﹣D的反应类型是 .
(2)Y的结构简式为 , 在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有种.
(3)C分子间可在一定条件下反应生成含有3个六元环的产物,该反应的化学方程式为 .
(4)由E转化为氯吡格雷时,生成的另一种产物的结构简式为 .
(5)写出A的所有同分异构体(芳香族化合物)的结构简式:(不考虑立体异构).
(6)请结合题中信息写出以 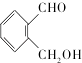 为有机原料制备化合物
为有机原料制备化合物 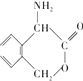 的合成路线流程图(无机试剂任选) . (合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选) . (合成路线流程图示例如下:CH3CH2OH ![]() CH=CH2
CH=CH2 ![]()
![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+ , 模拟装置如图所示,下列说法正确的是( ) 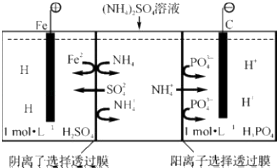
A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为:4OH﹣﹣4e═2H2O+O2↑
C.电解一段时间后,阴极室溶液中的pH升高
D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是( )
序号 | 电解质 | 酸 | 氧化物 | 单质 | 酸性氧化物 |
A | Cl2 | FeBr2 | CO | Hg(汞) | FeCl3 |
B | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
C | KClO3 | HCl | CaO | Cl2 | CO2 |
D | K2O | HCl(浓) | H2O | Cl2 | MnO2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料﹣﹣纳米氧化铜的重要前驱体之一,下面是它的一种实验室合成路线: 
制备苯乙酸的装置示意图如图(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)在250mL三口瓶a中加入70mL 70%硫酸,配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是;
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器b的作用是;仪器c的名称是 , 其作用是 , 反应结束后加适量冷水,再分离出苯乙酸粗品.加入冷水的目的是 , 下列仪器中可用于分离苯乙酸粗品的是(填标号) A、分液漏斗 B、漏斗 C、烧杯 D、直形冷凝管 E、玻璃棒
(3)提纯苯乙酸的方法是 , 最终得到44g纯品,则苯乙酸的产率是;
(4)用CuCl22H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是;
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同物质的量的SO2与SO3,下列说法正确的是( )
A.硫元素的质量比为5:4 B.原子总数之比为4:3
C.质量之比为1:1 D.分子数之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关0.1mol/LNa2S溶液的叙述正确的是( )
A.该溶液中存在两个平衡、七种粒子
B.该溶液中K+、NH ![]() 、NO
、NO ![]() 、Al3+可以大量共存
、Al3+可以大量共存
C.滴加少量稀硫酸,充分振荡无现象
D.通入足量SO2气体,发生反应的离子方程式:2S2﹣+SO2+2H2O═3S↓+4OH﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com