
【题目】下列离子方程式中书写正确的是
A.铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag
B.氧化铜溶于稀硫酸:O2-+2H+=H2O
C.氢氧化钠溶液与过量碳酸氢钙溶液反应:OH-+HCO3-+Ca2+=CaCO3↓+H2O
D.硫酸镁溶液与氢氧化钡溶液反应:Mg2++2OH-=Mg(OH)2↓
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】实验是学习化学的一个重要途径。
(1)图1是实验室常用的制气装置,其中b可用于制取O2和______(写化学式),其制取反应的化学方程式为_________。若用二氧化锰和浓盐酸制取氯气应选择的装置为_______,反应的离子方程式为__________。

(2)图2是实验室制备氯气并进行一系列相关实验的装置。

①A中盛放的固体药品是_________ (填化学式),装置B中盛装的液体试剂为_________。
②装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、II处依次放入的物质正确的是_________(填字母编号)。
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
③D中发生反应的离子方程式是_________。将装置D中的溶液加入装置E中,溶液分为两层,上层呈紫红色,要分离出紫红色溶液,需使用的玻璃仪器是玻璃棒、烧杯和________。
④报纸报道了多起因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。请用离子方程式表示其原因: ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(1)甲中SO42-移向________极(填“铝片”或“镁片”)。写出甲中负极的电极反应式____________。
(2)乙中负极为________,总反应的离子方程式:_______________。此反应中氧化剂和还原剂的物质的量之比为________,还原产物是________。
(3)原电池是把______________的装置。上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池中的正负极”这种做法________(填“可靠”或“不可靠”)。如不可靠,请你提出另一个判断原电池正负极的可行性实验方案________(如可靠,此空可不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海藻、海带中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室中从海藻中提取碘的流程如图:
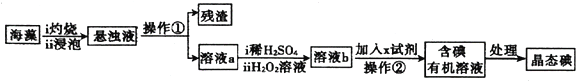
(1)溶液a中加入稀H2SO4、H2O2溶液后发生反应的离子方程式式为__________。
(2)上述流程中实验操作②的名称是__________。
(3)证明溶液b中含有单质碘的实验操作是__________。
(4)溶液b中加入的试剂X可以选择是__________。
A.酒精 B.苯 C.乙酸 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示:下列说法正确的是:
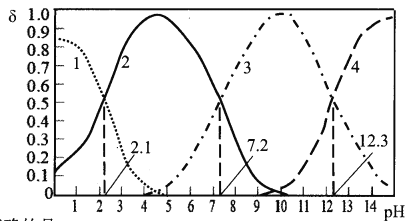
A. 曲线1和曲线2分别表示8(H3PO4)和6(HPO42-)的变化
B. 25℃时,H3PO4的电离常数K1=10-2.1
C. pH=7.2时,溶液中c(H2PO4ˉ)+c(HPO42-)+c(OHˉ)=c(Na+)+c(H+)
D. pH=12.3时,溶液中由水电离出的c(H+)=10-12.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物D,质谱图表明其相对分子质量为86,将8.6gD完全燃烧的产物依次通过装有浓硫酸和碱石灰的装置,浓硫酸中增重9g,碱石灰中增重22g.其相关反应如图所示,其中B、D、E的结构中均含有2个﹣CH3 , 它们的核磁共振氢谱中均出现4个峰.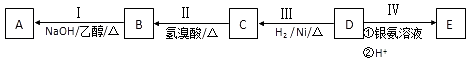
请回答:
(1)B中所含官能团的名称为;D的分子式为;
(2)Ⅲ的反应类型为(填字母序号);
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
Ⅰ:;
Ⅳ﹣:;
(4)C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个﹣CH3 , 它们的结构简式为和;
(6)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”,十九大再次强调环境保护的重要性。“绿色化学”的核心是实现污染物“零排放”。下列符合 “绿色化学”理念的是
A. 甲烷与氯气制备一氯甲烷
B. 用稀硝酸和铜反应制取Cu(NO3)2
C. 由反应2SO2+02![]() 2SO3制SO3
2SO3制SO3
D. 向铜和稀硫酸的溶液中加入H2O2制备硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )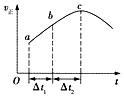
A.反应物的总能量低于生成物的总能量
B.△t1=△t2时,CO的转化率:a~b段小于bc段
C.反应在c点达到平衡状态
D.反应物浓度:a点小于b点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com