
【题目】工业上常用(NH4)2SO3溶液吸收废气中的SO2,室温下测得溶液中lgY[Y=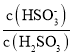 或
或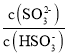 ],与pH的变化关系如图所示。则下列说法一定错误的是( )
],与pH的变化关系如图所示。则下列说法一定错误的是( )

A.通入少量SO2的过程中,直线Ⅱ中的N点向M点移动
B.α1=α2一定等于45°
C.直线Ⅱ中M、N点一定存在c2(HSO![]() )>c(SO
)>c(SO![]() )·c(H2SO3)
)·c(H2SO3)
D.当对应溶液的pH处于1.81<pH<6.91时,溶液中的一定存在:c(HSO![]() )>c(SO
)>c(SO![]() )>c(H2SO3)
)>c(H2SO3)
【答案】D
【解析】
H2SO3的第一电离常数远大于第二电离常数,K1>K2,当氢离子浓度相同时,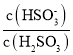 >
>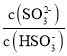 ,I>Ⅱ,I表示lg
,I>Ⅱ,I表示lg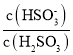 与pH变化的关系。
与pH变化的关系。
A.(NH4)2SO3溶液通入少量SO2的过程中,发生(NH4)2SO3+H2O +SO2=NH4HSO3,SO![]() 浓度减小,HSO
浓度减小,HSO![]() 浓度增大,
浓度增大,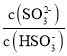 减小,直线Ⅱ中的N点向M点移动,故A正确;
减小,直线Ⅱ中的N点向M点移动,故A正确;
B.![]() ,则
,则![]() ,
,![]() ,同理可得
,同理可得![]() ,故α1=α2一定等于45°,故B正确;
,故α1=α2一定等于45°,故B正确;
C.过N、M点作垂线交I线,N、M的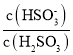 >
>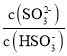 ,即pH相同时Ka1>Ka2,整理得:直线Ⅱ中M、N点一定存在c2(HSO
,即pH相同时Ka1>Ka2,整理得:直线Ⅱ中M、N点一定存在c2(HSO![]() )>c(SO
)>c(SO![]() )·c(H2SO3),故C正确;
)·c(H2SO3),故C正确;
D.pH=1.81时,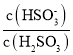 =1,c(HSO
=1,c(HSO![]() )=c(H2SO3),溶质为NH4HSO3和H2SO3,pH=6.91时,
)=c(H2SO3),溶质为NH4HSO3和H2SO3,pH=6.91时,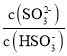 =1,c(HSO
=1,c(HSO![]() )=c(SO
)=c(SO![]() ),溶质为NH4HSO3和(NH4)2SO3,pH在1.81<pH<6.91变化的过程中,c(H2SO3)持续减小,c(SO
),溶质为NH4HSO3和(NH4)2SO3,pH在1.81<pH<6.91变化的过程中,c(H2SO3)持续减小,c(SO![]() )持续增大,c(HSO
)持续增大,c(HSO![]() )先增大后减小,但无法判断c(SO
)先增大后减小,但无法判断c(SO![]() )大于c(H2SO3);也可以从图中读出:当对应溶液的pH处于1.81<pH<6.91时,
)大于c(H2SO3);也可以从图中读出:当对应溶液的pH处于1.81<pH<6.91时,![]() <0、
<0、![]() >0,无法判断c(SO
>0,无法判断c(SO![]() )大于c(H2SO3);故D错误;
)大于c(H2SO3);故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】工业上由乙苯生产苯乙烯的反应如下,有关说法正确的是
![]()
A. 该反应的类型为取代反应
B. 可用溴水鉴别乙苯和苯乙烯
C. 乙苯分子中所有原子可能在同一平面
D. 比乙苯多一个碳原子的同系物R的同分异构体(包含R)共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下重水(D2O)的离子积常数为1.6×10-15,用定义pH一样来规定pD=-lg{c(D+)},则该温度下,下列叙述正确的是
A.纯净的重水(D2O)中,pD=7
B.1 L溶解有0.01 mol DCl的重水溶液,其pD=12.0
C.纯净的重水中,c(D+)=c(OD-)
D.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)NaClO2中Cl的化合价为_________;
(2)写出“反应”步骤中生成ClO2的化学方程式________________________;
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、_______________;
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应中,氧化剂与还原剂的物质的量之比为__________________,该反应中氧化产物是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与图所示一致的是( )
A.图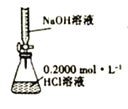 用于测定NaOH溶液的浓度
用于测定NaOH溶液的浓度
B.图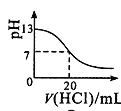 表示25
表示25![]() 时,用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
时,用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
C.图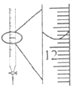 记录滴定终点读数为12.00 mL
记录滴定终点读数为12.00 mL
D.电导率是衡量电解质溶液导电能力大小的物理量,图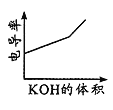 表示KOH溶液滴定CH3COOH溶液时溶液的电导率变化曲线示意图
表示KOH溶液滴定CH3COOH溶液时溶液的电导率变化曲线示意图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. H与O可形成既含极性共价键又含非极性共价键的化合物
B. 28g由 C2H4和 C3H6组成的混合物中,H原子的数目为4NA
C. 在D218O中,质量数之和是质子数之和的两倍
D. 1mol —CH3中含有的电子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O![]() CaO2·8H2O反应时通常加入过量的Ca(OH)2,其目的是 。
CaO2·8H2O反应时通常加入过量的Ca(OH)2,其目的是 。
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有____________(填序号)。
A.Ca2+ B.H+ C.CO32- D.OH
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,等MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
O2![]() MnO(OH)2
MnO(OH)2 ![]() I2
I2 ![]() S4O62
S4O62
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式 ;
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为 mg·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用核磁共振仪对分子式为C3H8O的有机物进行分析,核磁共振氢谱有三个峰,峰面积之比是1:1:6,则该化合物的结构简式为
A.CH3-O-CH2-CH3B.![]()
C.CH3CH2CH2OHD.C3H7OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病.治疗高血脂的新药I的合成路线如图所示:

已知:a. ;
;
b. RCHO
RCHO
请回答下列问题:
(1)反应①所需试剂、条件分别是____。
(2)A→B的化学方程式为____。
(3)G的结构简式为____。
(4)化合物W的相对分子质量比化合物C大14。且满足下列条件.W的可能结构有___种。
①遇FeCl3溶液显紫色 ②属于芳香族化合物 ③能发生银镜反应
其中核磁共振氢谱显示有5种不同化学环境的氢.且峰面积比为2:2:2:1:1的结构简式为___
(5)设计用甲苯和乙醛为原料制备![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)____。
目标产物)____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com