
某溶液中可能含有Na+、NH 、Ba2+、SO
、Ba2+、SO 、I-、S2-,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
、I-、S2-,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是( )
A.Na+ B.SO
C.Ba2+ D.NH
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为________,氧化性最弱的简单阳离子是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:_____________________________________________。
(2)[2013·广东理综,32(3)]完成煅烧过程中一个反应的化学方程式:________CuO+________Al2O3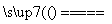 ________CuAlO2+________↑。
________CuAlO2+________↑。
查看答案和解析>>
科目:高中化学 来源: 题型:
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、NH 、Fe3+、Al3+、Cl-、OH-、NO
、Fe3+、Al3+、Cl-、OH-、NO 、S2-、CO
、S2-、CO 、SO
、SO 。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则N溶液里的阴离子一定有 ( )
。已知两溶液所含离子各不相同,N溶液里的阳离子只有两种,则N溶液里的阴离子一定有 ( )
A.OH-、CO 、S2- B.S2-、Cl-、SO
、S2- B.S2-、Cl-、SO
C.CO 、NO
、NO 、S2- D.Cl-、SO
、S2- D.Cl-、SO 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO 、SO
、SO 、Cl-、I-、HCO
、Cl-、I-、HCO ,取该溶液进行如下实验:
,取该溶液进行如下实验:
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴甲基橙溶液 | 溶液变红色 |
| ②取少量该溶液,加入铜片和浓硫酸,加热 | 有无色气体产生,遇空气可以变成红棕色 |
| ③取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断:
(1)溶液中一定存在的离子是________;溶液中肯定不存在的离子是____________________________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称(若为溶液反应,说明使用试剂的名称,不必写详细步骤)_________________________ _______________________________________________。
(3)写出实验⑤中所有反应的离子方程式: ________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中:Na+ 、K+、MnO 、CO
、CO
B.c(H+ )=1×10-13 mol·L-1的溶液中:Mg2+、Cu2+、SO 、NO
、NO
C.0.1 mol·L-1 NH4HCO3溶液中:K+ 、Na+ 、NO 、Cl-
、Cl-
D.0.1 mol·L-1 FeCl3溶液中:Fe2+ 、NH 、SCN-、SO
、SCN-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.1.8 g重水(D2O)中含有的质子数和电子数均为1.0NA
B.500℃ 30 MPa下,N2(g)+3H2(g)2NH3(g) ΔH=-38.6 kJ·mol-1。将分子数为1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3 kJ
C.标准状况下,将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA
D.15 g石英晶体中含有的Si—O键数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com