
下表是A、B、C、D、E、F六种短周期元素的部分化合价、电负性和原子半径数据.下列说法正确的是( )
| A | B | C | D | E | F |
化合价 | +1 | ﹣2 | ﹣1 | ﹣2 | ﹣1 | +1 |
电负性 | 2.1 | 2.5 | 3.0 | 3.5 | 4.0 | 0.9 |
原子半径/nm | 0.037 | 0.102 | 0.099 | 0.073 | 0.071 | 0.154 |
A.A的单质中含有金属键
B.F2D2含有非极性共价键
C.沸点:A2D<AE
D.最高价氧化物对应水化物的酸性:B>C
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:实验题
高铁酸钾是绿色、环保型水处理剂,也是高能电池的电极材料。工业上,利用硫酸亚铁为原料,通过铁黄(FeOOH)制备高铁酸钾,可降低生产成本且产品质量优。工艺流程如下:
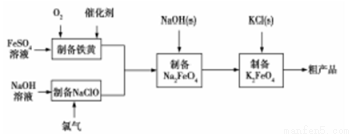
回答下列问题:
(1)有同学认为上述流程可以与氯碱工业联合。写出电解饱和食盐水制取次氯酸钠的化学方程式 。
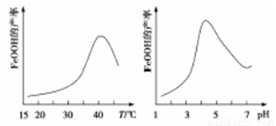
(2)制备铁黄的反应中氧化剂与还原剂的物质的量之比为 。实验测得反应溶液的pH、温度对铁黄产率的影响如图所示。反应温度宜选择 ;pH大于4.5时铁黄产率降低的主要原因可能是 。
(3)用高铁酸钾处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3、CN-等,生成的氢氧化铁胶体粒子还能吸附水中悬浮杂质。试写出高铁酸钾处理含CN-废水时除去CN-的离子方程式 。
(4)K2FeO4可作锌铁碱性高能电池的正极材料,电池反应原理:
2K2FeO4+3Zn+8H2O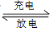 2Fe(OH)3+3Zn(OH)2+4KOH。放电时负极材料是 ;充电时阳极的电极反应式为 。
2Fe(OH)3+3Zn(OH)2+4KOH。放电时负极材料是 ;充电时阳极的电极反应式为 。
(5)已知:常温下,Kap[Fe(OH)3]=4.0×10-38。高铁酸钾的净水能力与废水的pH有关,当溶液pH=2时,废水中c(Fe3+)= mol·L-1。
(6)如果上述流程中,铁元素总利用率为75%。利用1mol 2mol·L-1FeSO4溶液能制备纯度为90%的高铁酸钾 kg。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
已知X(g)+3Y(g)═ 2Z(g)△H>0,下列对该反应的说法中正确的是( )
A.△S>0
B.逆向能自发进行,且反应速率和平衡常数均较大
C.反应物总能量大于生成物总能量
D.在任何温度下都不能自发进行
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)?NH3(g)+HI(g) ②2HI(g)?H2(g)+I2(g)达到平衡时,c(H2)=0.5mol•L﹣1,c(HI)=4mol•L﹣1,下列说法正确的是( )
A.平衡时,c(NH3)=6 mol•L﹣1
B.反应起始时固体NH4I是5 mol
C.平衡时HI的分解率为20%
D.改变反应起始固体NH4I的量,保持其他条件不变,平衡时各气体浓度也发生改变
查看答案和解析>>
科目:高中化学 来源:2017届河南信阳高考化学暑假自学自测专练:原子结构与性质(解析版) 题型:简答题
已知A原子只有一个未成对电子,M电子层比N电子层多11个电子,试回答下列问题:
(1)N电子层的s轨道和p轨道中只有一个未成对电子的元素有哪些?
(2)写出A原子的电子排布式和元素符号。
(3)指出元素A在周期表中的位置。
(4)指出元素A的最高化合价和最低化合价。
查看答案和解析>>
科目:高中化学 来源:2017届河南信阳高考化学暑假自学自测专练:原子结构与性质(解析版) 题型:选择题
下列说法正确的是( )
A. Na、Mg、Al的第一电离能逐渐增大
B. V、Cr、Mn的最外层电子数逐渐增大
C. S2﹣、Cl﹣、K+的半径逐渐减小
D. O、F、Ne的电负性逐渐增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下学期期末化学试卷(解析版) 题型:选择题
已知甲、乙、丙、丁四种物有如下转化关系,其中甲、乙、丁均能发生银镜反应,则甲为( )
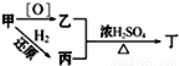
A、甲醇 B、甲醛 C、乙酸 D、乙醛
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省揭阳市高二期末统考理综化学试卷(解析版) 题型:填空题
[化学——选修5物质结构与性质]
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为 ,该元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4, B原子的杂化方式为 。
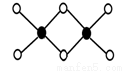
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“不是”)平面型分子。
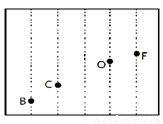
(4)依据第二周期元素第一电离能的变化规律,参照图中B、C、O、F元素的位置,用小黑点表示N元素的相对位置。
(5)Al单质为面心立方晶体,其晶体参数a=0.405nm,列式表示Al单质的密度: g·cm-3。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省锦州市高一下学期期末统考化学试卷(解析版) 题型:选择题
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。下列有关海水综合利用的说法不正确的是
A.从海水中提炼出的氘(含 HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题,
成为一条新的科学思路。HDO与 H2O化学性质相同
B.从海水中提取镁可以采用下列方法:
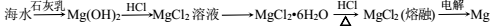
C.从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,已知该化合物中碘元素呈+3和+5两种价态,则这种化合物的化学式是 I4O9
D.除去粗盐中的 SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液 NaOH溶液
NaOH溶液 BaCl2溶液
BaCl2溶液 过滤后加盐酸
过滤后加盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com