
下表是元素周期表的一部分,有关说法不正确的是( )
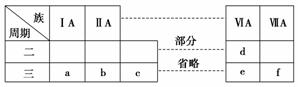
A.元素e的氧化物对应的水化物均为强酸
B.a、b、d、e四种元素的离子半径:e>d>a>b
C.b、f两种元素形成的化合物为离子化合物
D.a、c、e的最高价氧化物对应的水化物之间能够相互反应
科目:高中化学 来源: 题型:
据报道,我国拥有的完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供了服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A.正极反应式为O2+2H2O+4e-—→4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
温度为T时,向2.0 L 恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)====PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
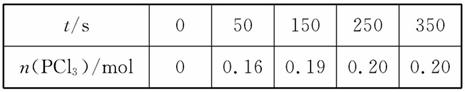
下列说法正确的是( )
A.反应在前50 s的平均速率
v(PCl3)=0.003 2 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol  PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,在pH=12的某溶液中,分别有甲、乙、丙、丁四位同学计算出由水电离出的[OH-]的数据分别为甲:1.0×10-7 mol· L-1;乙:1.0×
L-1;乙:1.0×
10-6 mol·L-1;丙:1.0×10-2 mol·L-1;丁:1.0×10-12 mol·L-1。其中你认为可能正确的数据是( )
A.甲、乙 B.乙、丙 C.丙、丁 D.乙、丁
查看答案和解析>>
科目:高中化学 来源: 题型:
现有含KCl、K2SO4和KNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-和NO3-的相互分离。相应的实验过程可用 如图表示:
如图表示:
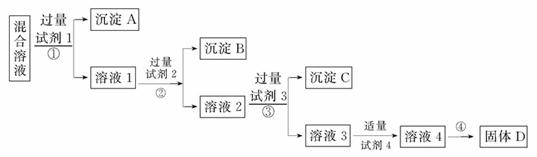
(1)写出上述实验过程中所用试剂的名称:
试剂1__________,试剂2__________,试剂4__________。
(2)恰当地控制试剂4的加入量的方法是____________________。
(3)加入过量试剂3的目的是______________________________。
(4)在加入试剂4后,获得固体D的实验操作④是__________ (填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W为四种短周期主族元素,原子序数依次增大。其中X、Z同主族,Y、Z同周期,Y原子的最外层电子数是次外层电子数的一半,X原子的最外层电子数是核外电子层数的3倍,W的最高正化合价与最低负化合价的代数之和为6。下列说法正确的是( )
A.X、Y、Z、W四种元素的简单氢化物中,W的氢化物的沸点最高
B.X、Y、Z三种元素的原子半径由大到小的顺序为Y>X>Z
C.Y、Z、W三种元素的非金属性由强到弱的顺序为W>Z>Y
D.Y、Z、W三种元素的最高价氧化物对应的水化物都是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)===2C3H5(ONO2)3(l)ΔH1
2H2(g)+O2(g)===2H2O(g)ΔH2
C(s)+O2(g)===CO2(g)ΔH3
则反应4C3H5(ONO2)3(l)===12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
( )
A.12ΔH3+5ΔH2-2ΔH1 B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1 D.ΔH1-5ΔH2-12ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
控制变量法在化学实验探究中运用较多,它是指在研究和解决问题的过程中,对影响事物变化规律的因素或条件加以人为控制,使其中的一些条件按照特定的要求发生或不发生变化,以便在研究过程中,找到事物变化发展的规律。根据因素和条件的性质,可分为实验变量(自变量)、反应变量(因变量)和无关变量。某研究小组用酸性KMnO4溶液与H2C2O4溶液反应中溶液紫色消失的方法,来研究浓度对化学反应速率的影响。下列实验有关变量控制的操作错误的是( )
A.为控制无关变量的影响,将实验温度均确定为25℃、酸性KMnO4溶液与H2C2O4溶液的体积均确定为4 mL,不使用催化剂
B.可选择浓度分别为0.05 mol·L-1、0.01 mol·L-1、0.001 mol·L-1的KMnO4酸性溶液和浓度均为0.001 mol·L-1的H2C2O4溶液反应,来操纵实验变量,进行对照实验
C.可将单位时间内反应所生成的CO2体积作为实验变量(自变量)进行本实验研究
D.该实验研究中的反应变量(因变量)是溶液紫色褪去所消耗的时间
查看答案和解析>>
科目:高中化学 来源: 题型:
1995年,化学家合成了一种分子式为C200H196,含有多个碳碳叁键的链烃.该分子中最多含有碳碳叁键( )
|
| A. | 49个 | B. | 50个 | C. | 51个 | D. | 53个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com