
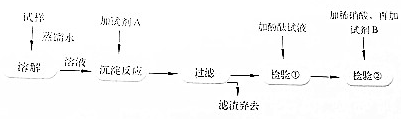
分析 试样加入蒸馏水溶解,加入试剂A生成沉淀,A可为Ba(NO3)2,生成沉淀为BaCO3,过滤后在滤液中加入酚酞,如变为红色,则说明含有NaOH,最后加入稀硝酸,在加入AgNO3,如生成沉淀,可说明含有NaCl,以此解答该题.
解答 解:(1)由以上分析可知A为Ba(NO3)2,目的是除去碳酸钠,以对实验产生干扰,故答案为:Ba(NO3)2;除去碳酸钠;
(2)检验①中加酚酞试液是检验NaOH,溶液呈红色,故答案为:NaOH;
(3)加入硝酸酸化,至溶液呈酸性,在加入硝酸银,可检验NaCl,如生成沉淀,说明含有NaCl,故答案为:呈酸性;AgNO3;NaCl.
点评 本题考查物质的检验和鉴别的实验方案的设计,为高频考点,侧重考查学生的分析能力和实验能力,注意把握物质的性质以及实验的合理性、可行性的评价,难度不大.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状态下,22.4LSO3含有原子数为4NA | |
| B. | 4℃时,18gH2O含有2NA 个非极性键 | |
| C. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| D. | 将含1molFeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
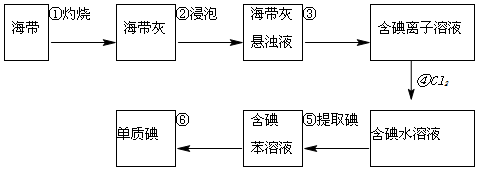 请填写下列空白:
请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
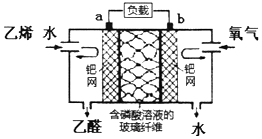
| A. | 该电化学装置是电解池 | |
| B. | a极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+ | |
| C. | 氧气在b极被氧化 | |
| D. | 电子移动方向:电极a→负载→电极b→磷酸溶液→电极a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+3Y?2Z | |
| C. | 改变温度可以改变此反应的平衡常数 | |
| D. | 增大压强使平衡向生成Z的方向移动,平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
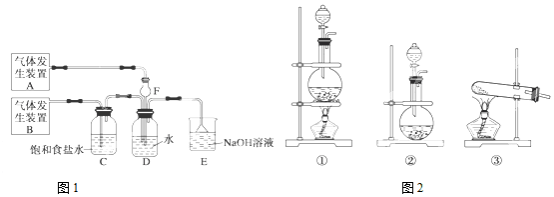
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

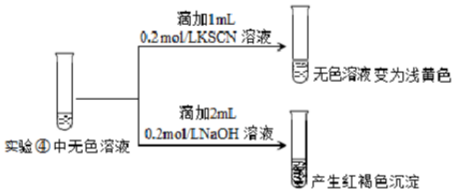
| 实验操作及现象 | ④向2mL0.2mol/L FeCl3溶液中滴入2mL1mol/LNaF溶液.溶液变无色 |
| ⑤向2mL0.2mol/L FeCl3溶液中滴入2mL蒸馏水,溶液颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H10含苯环的烃的同分异构体有3种 | |
| B. | 葡萄糖、蔗糖、淀粉在一定条件下都可发生水解反应 | |
| C. | C4H8→C4H7Cl的转化是取代反应 | |
| D. | 丙烯酸(CH2═CHCOOH)和山梨酸(CH3═CHCH═CHCOOH)互为同系物 |
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
下列类比关系正确的是
A.AlCl3与过量NaOH溶液反应生成AlO2—,则与过量NH3·H2O反应也生成AlO2—
B.Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应
C.Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3
D.Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com