
 某物质A在一定条件下加热分解,产物都是气体,分解方程式为2A
某物质A在一定条件下加热分解,产物都是气体,分解方程式为2A B+2C+2D。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为
B+2C+2D。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为
A.7d B.5d C.3d D.2d
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:选择题
某溶液中可能含有SO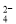 、CO
、CO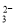 、Cl-。为了检验其中是否含有SO
、Cl-。为了检验其中是否含有SO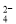 ,除BaCl2液外,还需要的溶液是 ( )
,除BaCl2液外,还需要的溶液是 ( )
A.H2SO4 B.HCl C.NaOH D.NaNO3
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:选择题
下列表示不正确的是( )
A.MgF2的电子式: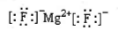
B.二甲醚的结构简式:CH3—O—CH3
C.NH3分子的比例模型:
D.氧原子(18O)的结构示意图: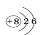
查看答案和解析>>
科目:高中化学 来源:2017届安徽省培优联盟高三冬季联赛化学试卷(解析版) 题型:选择题
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知四种元素的电子层数和最外层电子数之和均为10,且它们分别属于连续的四个主族。下列说法正确的 ( )
A. W、X、Y元素的简单离子对水的电离平衡的影响是相同的
B. Y的离子是其所在周期中半径最小的简单离子
C. X、Y、Z的最高价氧化物对应的水化物两两之间能反应
D. 工业上获得X、Y单质的方法主要是电解其熔融的氯化物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:填空题
⑴在含有Na+ 、Mg2+、HCO3ˉ、SO42ˉ的1L稀溶液中,它们的物质的量为2mol,1mol,2mol,1mol。
、Mg2+、HCO3ˉ、SO42ˉ的1L稀溶液中,它们的物质的量为2mol,1mol,2mol,1mol。
①向该溶液中滴加含0.5mol氢氧化钠的100mL溶液有关反应的离子方程式为:
②向该溶液中滴加含1.5mol氢氧化钠的100mL溶液有关反应的离子方程式为:
③向该溶液中滴加含3mol氢氧化钡的100mL溶液有关反应的离子方程式为:
⑵某电解质溶液中可能存在的离子为:Ag+、H+、Cu2+、CO32-、OHˉ、Clˉ你认为可以肯定存在的离子有: ,肯定没有的离子是: ,还需进一步确认的离子有: 确认的实验方法是: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:选择题
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是
A.2NaBr+Cl2 2NaCl+Br2
2NaCl+Br2
B.A lCl3+3NaAlO2
lCl3+3NaAlO2 +6H2O
+6H2O 4Al(OH)3↓+3NaCl
4Al(OH)3↓+3NaCl
C.2H2S+SO2 2H2O+3S↓
2H2O+3S↓
D.CaCO3 CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:选择题
下列溶液中的Cl-浓度与50mL 1mol·L-1氯化铝溶液中的Cl-浓度相等的是
A.150mL、1 mol·L-1 氯化钠溶液
B.75mL、2 mol·L-1 氯化铵溶液
C.150mL、1 mol·L-1 氯化钾溶液
D.75mL、1mol·L-1 氯化铝溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高二上期中化学卷(解析版) 题型:选择题
一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为49.6 g,当其缓慢经过无水CaCl2时,CaCl2增重25.2 g。原混合气体中CO2的质量为( )
A. 12.5 g B. 13.2 g C. 19.7 g D. 24.4 g
查看答案和解析>>
科目:高中化学 来源:2017四川省自贡市高三第一次诊断考试化学试卷(解析版) 题型:填空题
从某废液(含有Fe2+、Cu2+、Cl-)中回收铜并制得纯净的FeCl3溶液。现以制得纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如下:

已知:高锰酸钾(K2FeO4)位暗紫色固体,可溶于水。在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。高锰酸钾具有强氧化性。高锰酸钾(K2FeO4)与水作用产生Fe(OH)3。
(1)检验废液中含有Fe2+选用的试剂是________(填化学式);从废液中制得纯净的FeCl3溶液加入的试剂除铁粉外,还需要一种试剂是_________(填化学式),加入时发生反应的离子方程式为__________。
(2)高锰酸钾(K2FeO4)在处理水过程中的作用是_________和__________。
(3)“氧化”过程反应的离子方程式为__________。
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和________,上述工艺得到的高锰酸钾常含有杂志,可用重结晶法提纯,操作是:将粗产品用_________溶解,然后________。
(5)用回收的铜为原料可制得粗制CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂志的方法是:向溶液中加入H2O2,再调解溶液PH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO4·5H2O的晶体。
已知:室温时一些物质的Kaq如下表:
化学式 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
Kaq | 8.0×10-16 | 8.0×10-18 | 8.0×10-20 |
已知溶液中的离子浓度小于1×10-6mol·L-1时就认定沉淀完全。
加双氧水的目的是__________;若溶液中CuSO4的浓度为3.0mol·L-1,通过计算说明此方法可除去粗制CuSO4·5H2O晶体中FeSO4·7H2O的理由________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com