
【题目】有标准状况下的H2、Cl2混合气aL,经光照反应后,所得气体恰好能使b molNaOH完全转变成盐。那么a和b的关系不可能是()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。请回答下列问题:
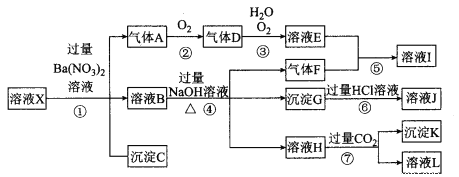
(1)依题意不进行实验即可判断溶液X中一定不存在的离子有 。
(2)下列结论正确的是 (填序号)。
A.X中肯定存在Fe2+、Al3+、NH4+
B.气体F经催化氧化可直接生成气体D
C.沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀K可能有Al(OH)3
D.溶液X中,一定没有NO3-
(3)产生气体A的离子方程式为 。
(4)转化⑥发生反应的现象为 。
(5)转化③中氧化剂与还原剂的物质的量之比为 。
(6)对不能确定是否存在的离子,如何确定其是否存在? (简述操作过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.
(1)第四周期过渡元素的明显特征是形成多种多样的配合物
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5].羰基镍[Ni(CO)4].CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式).
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列 .
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的.镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 .
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 .
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素的原子序数依次增大.已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个.试回答:
(1)写出下列元素的符号A ,D ,E ;
(2)用电子式表示B、F形成的化合物 ;
(3)A、C两种元素最高价氧化物的水化物之间反应的离子方程式 ;
(4)D的固态氧化物是 晶体.含n mol D的氧化物的晶体中含D﹣0共价键为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 氯化钠可用于制备纯碱
B. 食品袋中常放有生石灰,能起到抗氧化剂的作用
C. 大力推广矿物脱硫技术能减少酸雨危害
D. 石油裂解、煤的干馏、玉米酿酒、蛋白质变性都属于化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语回答下列问题:
(1)画出S2﹣的结构示意图: .
(2)写出氨气分子的电子式: .
(3)写出氮气分子的结构式 .
(4)苯酚钠溶液与过量CO2反应的化学方程式 .
(5)CH3CHO与银氨溶液反应的化学方程式: .
(6)CH2=CH﹣COOCH3在一定条件下发生加聚反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用Na2SO3还原MnO4-,如果还原含有2.4×10-3 mol MnO4-的溶液时,消耗18 mL0.2mol/L的Na2SO3 溶液,则Mn元素在还原产物中化合价为( )
A. +2 B. +4 C. +5 D. +6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com