
分析 (1)氯气有强氧化性,能氧化溴离子生成溴单质,还原剂失电子化合价升高而发生氧化反应;
(2)溴有氧化性,二氧化硫有还原性,在水溶液里,二氧化硫和溴发生氧化还原反应;
(3)用于萃取实验的仪器是分液漏斗,萃取剂的选取标准是:溶质在萃取剂中的溶解度大于在水中的溶解度,萃取剂和原溶剂不互溶,萃取剂和溶质不反应.
解答 解:(1)氯气有强氧化性,能氧化溴离子生成溴单质,自身被还原生成氯离子,反应方程式为:Cl2+2NaBr=Br2+2NaCl;Br2+3CO32-=BrO3-+5Br-+3CO2↑中Br2的化合价由0价变为+5价和-1价,所以Br2是氧化剂发生还原反应,也是还原剂发生氧化反应,还原剂为Br2;
故答案为:Cl2+2NaBr=Br2+2NaCl;Br2;
(2)溴有氧化性,二氧化硫有还原性,在水溶液里,二氧化硫和溴发生氧化还原反应生成硫酸和氢溴酸,反应方程式为:Br2+SO2+2H2O=2HBr+H2SO4;
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(3)用于萃取实验的仪器是分液漏斗,萃取剂的选取标准是:溶质在萃取剂中的溶解度大于在水中的溶解度,萃取剂和原溶剂不互溶,萃取剂和溶质不反应,根据萃取剂的选取标准知,乙醇、硝酸都和水互溶,所以不能作萃取剂,能作萃取剂的是四氯化碳;
故答案为:分液漏斗;②.
点评 本题考查物质的分离与提纯方法的综合应用,为高频考点,题目难度较大,试题涉及的知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力,明确实验原理为解答关键,注意熟练掌握化学实验基本操作方法.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 氯气的氧化性 | 将湿润的淀粉KI试纸放于充满Cl2的集气瓶口,试纸变蓝 |
| B | 配制480mL 0.2mol/L NaOH溶液 | 准确称量NaOH固体4.0g溶于水,配制成500mL溶液 |
| C | 比较H2CO3和H2SO4的酸性强弱 | 室温下,用pH试纸测定浓度为 0.1mol/L Na2CO3溶液和 0.1mol/L Na2SO4溶液的pH |
| D | 鉴别Na2CO3溶液与NaHCO3溶液 | 分别加入Ca(OH)2溶液看是否产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )
如图是元素周期表的一部分,表格中所示元素均为前四周期的元素.X元素的非金属性在同周期中仅次于一种元素.下列说法中不正确的是( )| A. | X代表的元素处于第ⅥA族 | |
| B. | Y的最低负化合价是-3 | |
| C. | M元素的最高价氧化物对应的水化物的化学式是HMO3 | |
| D. | 气态氢化物的稳定性:N>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )| A. | 保护 1mol 醛基时也可用2molCH3CH2OH | |
| B. | 合成 1mol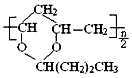 需要 1mol 需要 1mol 和 nmolCH3CH2CH2CHO 和 nmolCH3CH2CH2CHO | |
| C. | 通过上述反应合成的 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 | |
| D. | 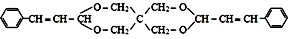 可由 C(CH2OH)4 与 可由 C(CH2OH)4 与 通过上述反应得到 通过上述反应得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向浓氨水中滴加饱和 FeCl3溶液,可以制得 Fe(OH)3胶体 | |
| B. | 为除去Mg(OH)2固体中少量Ca(OH)2,可用饱和 MgCl2溶液多次洗涤,再水洗、干燥 | |
| C. | 向溶液X中加入足量盐酸,产生无色无味气体,将气体通入澄清石灰水,产生白色沉 淀,说明溶液 X 中含有 CO32- | |
| D. | 卤代烃Y与NaOH醇溶液共热后,恢复至室温,再滴加AgNO3溶液,产生白色沉淀,说明卤代烃 Y 中含有氯原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除(3)外 | B. | 除(4)外 | C. | 除(2)外 | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com