
【题目】化合物M是一种具有茉莉花香味的无色油状液体,结构简式是![]() ,其合成路线如下(部分反应条件未注明):
,其合成路线如下(部分反应条件未注明):

(1)烃A的结构简式是________________,C所含官能团的名称是_____________。
(2)为检验F中的官能团,可选用的试剂是____________________。
(3)E→F反应的化学方程式是______________________。
【答案】![]() 羟基 新制的银氨溶液或氢氧化铜悬浊液 2CH3CH2OH+O2
羟基 新制的银氨溶液或氢氧化铜悬浊液 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
![]() 可以看成是苯甲醇与乙酸经酯化反应后的生成物,A在光照的条件下与氯气发生烷基上的取代反应生成B(C7H7Cl),则A是甲苯,结构简式是:
可以看成是苯甲醇与乙酸经酯化反应后的生成物,A在光照的条件下与氯气发生烷基上的取代反应生成B(C7H7Cl),则A是甲苯,结构简式是:![]() ,A在氯气光照的条件生成下B是
,A在氯气光照的条件生成下B是![]() ,B在碱性条件下水解生成C(
,B在碱性条件下水解生成C(![]() ),G为乙酸,逆推可知F为乙醛,E为乙醇,D为乙烯,由此分析。
),G为乙酸,逆推可知F为乙醛,E为乙醇,D为乙烯,由此分析。
(1)烃A是甲苯,结构简式是![]() ,C的结构简式是
,C的结构简式是![]() ,所含官能团的名称是羟基;
,所含官能团的名称是羟基;
(2) F为乙醛,官能团是醛基,用新制的银氨溶液或氢氧化铜悬浊液检验;
(3)E→F是乙醇催化氧化为乙醛,化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对于2SO2(g)+O2(g)![]() 2SO3(g) △H<0的反应,下列装置示意图中的实验不能达到目的是( )
2SO3(g) △H<0的反应,下列装置示意图中的实验不能达到目的是( )
A. 研究压强对反应的影响(p2>p1)
研究压强对反应的影响(p2>p1)
B. 研究温度对反应的影响
研究温度对反应的影响
C. 研究平衡体系中增加O2浓度对反应的影响
研究平衡体系中增加O2浓度对反应的影响
D. 体积恒定的密闭容器中催化剂对反应的影响
体积恒定的密闭容器中催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在画某种原色的一种单核微粒的结构示意图时,忘记在圆圈内标出其核电荷数,请你根据下面的提示做出自己的判断。
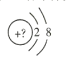
(1)若该微粒是电中性微粒,这种微粒的元素符号是_____________。
(2)若该微粒的还原性很弱,失去1个电子后变为原子,该原子的单质氧化性很强,该单质与水反应的 化学方程式为______________。
(3)若该微粒的氧化性很弱,得到1个电子后变为原子,该原子的单质还原性很强,该单质在氧气中燃烧所得产物的化学式为_______________。
(4)若该微粒的还原性很弱,失去2个电子后变成原子,其氢化物的结构式为_____________。
(5)若该微粒的符号为X3+,其氢氧化物与强碱反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的结构简式为![]() ,请回答下列问题.
,请回答下列问题.
(1)A中所含官能团的名称是_______、______;
(2)A可能发生的反应有______(填序号);
①取代反应 ②消去反应 ③水解反应 ④酯化反应
(3)将A与氢氧化钠的乙醇溶液混合并加热,再让得到的主要产物发生加聚反应,生成了某聚合物,该聚合物的结构简式是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量![]() ,较多的
,较多的![]() 及部分污泥,通过下列流程可从该废水中回收
及部分污泥,通过下列流程可从该废水中回收![]() 晶体及金属Cu。
晶体及金属Cu。

![]() 固体混合物是______
固体混合物是______![]() 填化学式
填化学式![]() ,试剂乙为______
,试剂乙为______![]() 填物质名称
填物质名称![]()
![]() 步骤3中发生反应的离子方程式为______
步骤3中发生反应的离子方程式为______
![]() 步骤4中涉及的操作是:蒸发浓缩、______、过滤、洗涤、干燥;蒸发浓缩、过滤操作中均用到的玻璃仪器是______
步骤4中涉及的操作是:蒸发浓缩、______、过滤、洗涤、干燥;蒸发浓缩、过滤操作中均用到的玻璃仪器是______
![]() 粗铜中常混有少量氧化亚铜
粗铜中常混有少量氧化亚铜![]() ,氧化亚铜与稀硫酸反应,会产生单质铜,同时溶液变蓝。试写出该反应的离子方程式______。
,氧化亚铜与稀硫酸反应,会产生单质铜,同时溶液变蓝。试写出该反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在指定条件下电离方程式正确的是( )
A. Na2CO3溶于水:Na2CO3===Na22++CO32-
B. Al(OH)3酸式电离:Al(OH)3===AlO2-+H2O+H+
C. NaHS溶于水HS-的电离:HS-+H2O![]() H2S+OH-
H2S+OH-
D. NaHSO4加热熔化:NaHSO4===Na++HSO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加徳罗常数的值,下列说法正确的是
A. 常温下,1L pH=13的Ba(OH)2溶液中OH-数为0.2NA
B. 2.4g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA
C. 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA
D. 0.lmol/L(NH4)2SO4溶液与0.2mol/LNH4Cl溶液中的NH4+数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和1mol O2,乙中充入4 mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)![]() 2SO2(g)+ O2(g)。下列有关说法正确的是
2SO2(g)+ O2(g)。下列有关说法正确的是
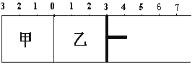
A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲
B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度: c(SO3)乙>2c(SO3)甲
C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ(SO2)乙>2ψ(SO2)甲
D.若活塞固定在7处不动,达平衡时两容器中SO3的物质的量分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.明矾和Ba(OH)2溶液反应至硫酸根沉淀完全的离子方程式:Al3++![]() +Ba2++3OH-=Al(OH)3↓+BaSO4↓
+Ba2++3OH-=Al(OH)3↓+BaSO4↓
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.向NaAlO2溶液通过量CO2制Al(OH)3:CO2+![]() +2H2O=Al(OH)3↓+
+2H2O=Al(OH)3↓+![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com