
下列离子方程式正确的是( )
|
| A. | 乙酸与碳酸钠溶液反应:2H++CO32﹣═CO2↑+H2O |
|
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO﹣+2H2O |
|
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O﹣+CO2+H2O |
|
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH﹣ |
考点:
离子方程式的书写.
专题:
离子反应专题.
分析:
A.乙酸是弱电解质应保留化学式;
B.醋酸溶液与新制氢氧化铜反应生成醋酸铜和水,注意醋酸和氢氧化铜都不能拆;
C.苯酚钠溶液中通入少量二氧化碳生成物为苯酚和碳酸氢钠,不符合反应的客观事实;
D.甲醛溶液与足量的银氨溶液共热发生银镜反应,注意1mol甲醛消耗4mol银氨络合物.
解答:
解:A.乙酸与碳酸钠溶液反应离子方程式:2CH3COOH+CO32﹣═CO2↑+2CH3COO﹣+H2O,故A错误;
B.醋酸溶液与新制氢氧化铜反应方程式:2CH3COOH+Cu(OH)2→Cu2++2CH3COO﹣+2H2O,故B正确;
C.苯酚钠溶液中通入少量二氧化碳离子方程式为:C6H5O﹣+CO2+H2O C6H5OH+HCO3﹣,故C错误;
C6H5OH+HCO3﹣,故C错误;
D.甲醛溶液与足量的银氨溶液共热离子方程式为:HCHO+4[Ag(NH3)2]++4OH﹣ CO32﹣+2NH4++4Ag↓+6NH3+2H2O,故D正确;
CO32﹣+2NH4++4Ag↓+6NH3+2H2O,故D正确;
故选:BD.
点评:
本题考查了离子方程式书写及正误判断,题目难度不大,易错选项C、D.注意苯酚钠和碳酸反应的实质、甲醛的结构特点是解题的关键.


科目:高中化学 来源: 题型:
Ⅰ.如图1为向25mL 0.1mol•L﹣1NaOH溶液中逐滴滴加0.2mol•L﹣1CH3COOH溶液过程中溶液pH的变化曲线.请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项 (选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 石蕊 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
(3)AB区间,c(OH﹣)>c(H+),则c(OH﹣)与c(CH3COO﹣)大小关系是 .
A.c(OH﹣)大于c(CH3COO﹣) B.c(OH﹣)小于c(CH3COO﹣)
C.c(OH﹣)等于c(CH3COO﹣) D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO﹣)+c(CH3COOH) 2c(Na+)(填“>”“<”或“=”).
Ⅱ.t℃时,某稀硫酸溶液中c(H+)=10﹣amol•L﹣1,c(OH﹣)=10﹣bmol•L﹣1,已知a+b=13:
(5)该温度下水的离子积常数Kw的数值为 .
(6)该温度下(t℃),将100mL 0.1mol•L﹣1的稀H2SO4与100mL 0.4mol•L﹣1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH= .
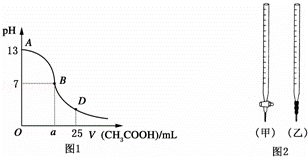
查看答案和解析>>
科目:高中化学 来源: 题型:
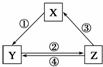
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是()
选项 X Y Z 箭头上所标数字的反应条件
A CaO Ca(OH)2 CaCO3 ①常温遇水
B AlCl3 NaAlO2 Al(OH)3 ②通入CO2
C Na2CO3 NaOH NaHCO3 ④过量Ca(OH)2溶液
D Cl2 Ca(ClO)2 HClO ③加浓盐酸
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
1﹣丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )
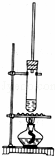
|
| A. | 不能用水浴加热 |
|
| B. | 长玻璃管有冷凝回流作用 |
|
| C. | 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
|
| D. | 加入过量乙酸可以提高1﹣丁醇的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(﹣OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
为了比较①H﹣OH,②CH3COOH,③CH3CH2﹣OH,④H2CO3,⑤苯酚五种物质分子中﹣OH上氢原子的活动性顺序,某课外活动小组设计了如下表所示的实验方案.请你利用有关实验仪器及给出的试剂,填写表中的空格,完成上述实验方案.可供选用的试剂有:紫色石蕊试液、金属钠、氢氧化钠溶液、碳酸钠溶液.实验中所需仪器自选.
| 实验步骤和操作 | 实验现象 | 结论(﹣OH上氢原子活动性顺序) |
| (1)五种物质各取少量于五支试管中,各加入紫色石蕊试液2~3滴 | ②④变红,其它不变 | ②、④>①、③、⑤ |
| (2) | ||
| (3)①、③、⑤各取少量于试管中,各加入少量NaOH溶液 | ⑤由浑浊变澄清 | ⑤>①、③ |
| (4) |
(5)通过以上实验比较,从而得出这五种物质分子中﹣OH上氢原子的活动性由强到弱的顺序为 (填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298K时,Mg(OH)2的溶度积常数KSP=5.6×10-12,取适量的MgCl2溶液,
加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是
A.所得溶液中的c (H+)=10-13mol/L
B.所得溶液中由水电离产生的c (OH-)=10-13 mol/L
C.所加的烧碱溶液的pH=13.0
D.所得溶液中的c (Mg2+)=5.6×10-10 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,在2X(g)+Y(g)2Z(g)的平衡体系中,X、Y、Z的浓度分别是2 mol·L-1,0.8 mol·L-1,2.4 mol·L-1,则Y在起始时的浓度可能是( )
A.0.8~2 mol·L-1 B.0~2 mol·L-1
C.0~0.8 mol·L-1 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
现有①BaCl2 ②金刚石 ③KOH ④H2SO4 ⑤干冰 ⑥碘片 ⑦晶体硅 ⑧金属铜 八种物质,按下列要求回答:(填序号)
(1)熔化时不需要破坏化学键的是 ,熔化时需要破坏共价键的是 ,熔点最高的是 ,熔点最低的是 .
(2)属于离子化合物的是 ,只有离子键的物质是 ,晶体以分子间作用力结合的是 .
(3)请写出③的电子式 ,⑤的电子式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com