
| A、.粉末中一定有Na20、Na202、NaHC03 |
| B、.粉末中一定不含有Na2C03和NaCl |
| C、粉末中一定不含有Na20和NaCl |
| D、.无法确定 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、对装置①,双手移去后,导管中水面高于烧杯内水面 |
| B、对装置②,长颈漏斗内液面高度保持不变 |
| C、对装置③,长导管内形成一段水柱 |
| D、对装置④,上下移动a管后,a、b两端液面仍相平 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、加入适量酸化的AgNO3溶液只发生复分解反应 |
| B、X中一定有Fe3+ |
| C、将操作顺序调换,现象一致,可判断X为FeBr3 |
| D、X一定为FeBr2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
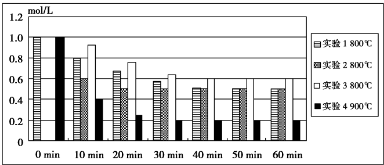
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大 | B、减小 |
| C、不变 | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、②④⑤ |
| C、②③⑤⑦ | D、②③④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com