
| A、①⑤ | B、①④ | C、②③⑥ | D、①⑤⑥ |
| ||
| ||


科目:高中化学 来源: 题型:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 | C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
| A、C7H16 |
| B、C7H14O2 |
| C、C8H18 |
| D、C8H18O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钾钠合金和钠的熔点 | B、纯水在80℃和25℃的pH | C、等物质的量的N2和H2在一定条件下反应,两者的转化率 | D、25℃时pH=11的Na2CO3溶液和pH=11的NaOH溶液中的水的电离度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过氧化钠能与二氧化碳反应,可用作呼吸面具的供氧剂 | B、氧化铝的熔点高,可用于制作耐高温仪器 | C、二氧化硅有导电性,可用于制作光导纤维 | D、石灰石是制水泥和玻璃的主要原料之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、依据丁达尔现象可将分散系分为溶液、胶体与浊液 | B、二氧化硅的分子式是SiO2 | C、单质硅是将太阳能转变为电能的常用材料 | D、漂白粉和水玻璃长期暴露在空气中变质,能用同一原理解释 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:实验题
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
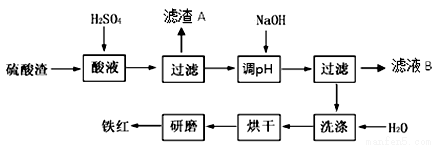
(1)硫酸渣的成分中属于两性氧化物的是 , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_________;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)滤渣A的主要成分为 ,滤液B可以回收的物质有Na2SO4、MgSO4和___________;
(4)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为 (用最简分数表达式表示)。
查看答案和解析>>
科目:高中化学 来源:2015届广东省海珠等四区高三联考理综化学试卷(解析版) 题型:选择题
室温下,下列溶液的离子浓度关系正确的是
A.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
B.NaHSO4溶液:c(H+)=c(SO42-)十c(OH-)
C.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
D.pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:实验题
(16分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
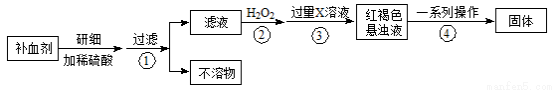
请回答下列问题:
(1)补血剂存放时间较长会氧化变质,对滤液中铁元素的存在形式提出如下假设:
假设1:只有Fe2+
假设2:只有Fe3+
假设3: 。
(2)如何证明步骤①滤液中含有Fe2+ 。
(3)步骤④中一系列处理的操作步骤: 、洗涤、灼烧、 、称量。
(4)该小组有些同学认为可用酸化的KMnO4溶液滴定进行Fe2+含量的测定。
①用离子方程式表示该滴定原理:____________________
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、量筒、药匙、胶头滴管外,还需 。
重复滴定三次,消耗1.00 mol/L KMnO4标准溶液体积分别为19.98 mL、20.00 mL、20.02mL,3次实验所用Fe2+溶液的体积为20.00 mL。请根据以上数据,再设计合理数据,完成下列实验过程的记录表格。(必须填满)
实验编号 | Fe2+溶液的 体积/mL |
|
|
|
1 | 20.00 |
|
|
|
2 | 20.00 |
|
|
|
3 | 20.00 |
|
|
|
③如何判断达到滴定终点:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com