


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:单选题
| 选项 | 试剂丙 | 甲离子 | 乙离子 |
| A | 稀硝酸、BaCl2溶液 | SO42- | SO32- |
| B | AgNO3溶液 | Cl- | I- |
| C | KSCN溶液 | Fe2+ | Fe3+ |
| D | 稀氨水 | Al3+ | Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
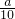 g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol?L-1的KMnO4溶液滴定,达到终点时消耗了25.00mL KMnO4溶液.查看答案和解析>>
科目:高中化学 来源: 题型:单选题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A | B | C | D | E | F | |
| A | ↓ | ↓ | - | ↓ | ↓ | |
| B | ↓ | - | - | ↑ | - | |
| C | ↓ | - | - | - | ↓ | |
| D | - | - | - | - | - | |
| E | ↓ | ↑ | - | - | ↓ | |
| F | ↓ | - | ↓ | - | ↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com