
【题目】下列有关元素的叙述,不正确的是( )
A. 氧元素是最基本的元素 B. DNA和磷脂都含有P元素
C. 核酸中的N元素存在于碱基中 D. 蛋白质中的N元素主要存在于肽键中
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态硼原子的价电子轨道表达式是_______________。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为___________。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的________。
(3)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为________。

②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______,写出一种与氨硼烷互为等电子体的分子_____(填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH![]() 的键角是________,立体构型为___________。
的键角是________,立体构型为___________。
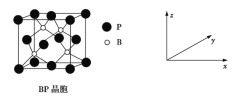
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是_______;已知晶胞边长为458 pm,则磷化硼晶体的密度是____g·cm-3(列式并计算,结果保留两位有效数字,已知4.583=96.07)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G为原子序数依次增大的短周期主族元素。B、C、D均能与A形成10电子分子,E单质可用于野外焊接钢轨的原料,F与D同主族。
(1)D、E、F的离子半径由大到小的顺序为___________(填离子符号)。
(2)写出能证明G比F非金属性强的一个化学方程式:_____________。
(3)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2:1:6,甲的电子式为_____,该反应的化学方程式为______________。
(4)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为________。常温下,液体乙与气体丙反应生成两种无污染的物质,该反应的氧化产物与还原产物的物质的量之比为________。
(5)现取100 mL1 mol/L的E的氯化物溶液,向其中加入1 mol/L NaOH溶液产生了3.9 g沉淀,则加入的NaOH溶液体积可能为____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B. 将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C. 向盐酸中加入氨水至中性,溶液中![]() >1
>1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中不![]() 变
变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸在下列用途或反应中所表现的性质(用字母填在横线上)。
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性
① 浓硫酸可用作气体干燥剂 __________;
② 往晶体硫酸铜中加浓硫酸,晶体变白___________;
③ 浓硫酸与铜反应__________;
④ 运用铁制槽车和铝制槽车运输浓硫酸_________;
⑤ 浓硫酸使润湿蓝色石蕊试纸先变红后又变黑___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pAg=-lg c(Ag+),Ksp(AgCl)=1×10-12。如图是向10 mL AgNO3溶液中逐渐加入0.1 mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位:mL)变化的图像(实线)。根据图像所得下列结论不正确的是( )

A. 原AgNO3溶液的物质的量浓度为1 mol·L-1
B. 图中x点的坐标为(100,6)
C. 图中x点可认为溶液中Ag+被沉淀完全
D. 把0.1 mol·L-1 NaCl换成0.1 mol·L-1 NaI,则图像在终点后变为虚线部分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“组成不同生物的元素含量有不同”。对此现象的合理解释是( )
A. 组成细胞的化学元素在含量上具有差异性
B. 生物界与非生物界在元素含量上具有差异性
C. 生物根据自身生命活动的需要,有选择地从环境中吸收的元素
D. 生物体内元素的存在形式各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有A、B、C三种元素,A、C元素原子的最外层电子数分别为6、2,B元素原子的最外层电子数是内层电子数的2倍,A原子比B原子多一个电子层,这三种元素分别为
A.Se Si BeB.O C MgC.O Si Ca D.S C He
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学课外活动小组利用以下装置完成系列实验.请回答以下问题:
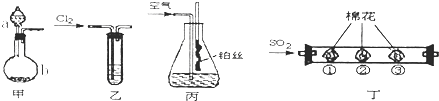
(1)装置甲中仪器a的名称为___ . 用装置甲制取NH3 , 在b中加入CaO固体,a中加入浓氨水,写出反应的化学方程式:___ .
(2)将C12持续通入装有淀粉一KI无色溶液的装置乙中,溶液变蓝而后逐渐褪色.查阅资料得知:溶液蓝色逐渐褪色,是因为有+5价的碘元素生成.请写出该反应的离子方程式:___ .
(3)用装置丙模拟“氨的催化氧化”实验.锥形瓶内装有浓氨水,通入空气,并将红热的铂丝插入锥形瓶内,铂丝保持红热.铂丝保持红热的原因是___;锥形瓶内还可观察到现象是___ .
(4)活动小组从“绿色化学”角度出发.在装置丁中进 行SO2的性质实验.其中棉花上蘸有不同试剂.请填写表中空白:
棉花位置 | ① | ② | ③ |
棉花上蘸有的试剂 | 品红溶液 | 酸性高锰酸钾溶液 | ___ |
现象 | ___ | 溶液紫色褪去 | 无 |
结论 | SO2具有漂白性 | SO2具有___ | SO2有毒,不能排空 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com