
| A. | 混合气体中N0的物质的量为0.01mol | |
| B. | 混合气体中N02的物质的量为0.02mol | |
| C. | 稀硝酸的浓度为0.045mol/L | |
| D. | 氢氧化钠溶液的浓度为0.1mol/L |
分析 336mL N0和NO2的物质的量为:$\frac{336×1{0}^{-3}L}{22.4L/mol}$=0.015mol,向混合气体中加入336mL NH3的物质的量为:0.015mol,恰好完全反应根据得失电子守恒可知:2n(N0)+4n(NO2)=3n(NH3),即2n(N0)+4n(NO2)=0.045①,而n(N0)+n(NO2)=0.015mol②,①②联立解之得n(N0)=0.0075mol;n(NO2)=0.0075mol,所以参加反应的锌的质量为:2n(Zn)=3n(N0)+n(NO2)=0.03mol,所以n(Zn)=0.015mol,由此分析解答.
解答 解:336mL N0和NO2的物质的量为:$\frac{336×1{0}^{-3}L}{22.4L/mol}$=0.015mol,向混合气体中加入336mL NH3的物质的量为:0.015mol,恰好完全反应根据得失电子守恒可知:2n(N0)+4n(NO2)=3n(NH3),即2n(N0)+4n(NO2)=0.045①,而n(N0)+n(NO2)=0.015mol②,①②联立解之得n(N0)=0.0075mol;n(NO2)=0.0075mol,所以参加反应的锌的质量为:2n(Zn)=3n(N0)+n(NO2)=0.03mol,所以n(Zn)=0.015mol,
A、混合气体中N0的物质的量为0.0075mol,故A错误;
B、混合气体中N02的物质的量为0.0075mol,故B错误;
C、稀硝酸的浓度为$\frac{(0.0075+0.0075+0.015×2)mol}{0.1L}$=0.45mol/L,故C错误;
D、根据反应方程式:2NO2+2Na0H═NaNO3+NaNO2+H20;NO2+N0+2Na0H═2NaNO2+H20,产物中氮与钠之比为1:1,所以氢氧化钠溶液的浓度为$\frac{0.0075×2}{0.15}$=0.1mol/L,故D正确;
故选D.
点评 本题考查化学方程式的计算,侧重考查分析计算能力,利用原子守恒能化繁为简,提高解题正确率,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KClO3和SO3溶于水后能导电,故KClO3和SO3均为电解质 | |
| B. | 升高温度能够增大单位体积内活化分子百分数,从而加快反应速率 | |
| C. | 中和热测定实验中需要用到的玻璃仪器有烧杯、温度计和量筒三种 | |
| D. | 强电解质的导电能力一定比弱电解质强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②⑤ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O | B. | NaCl+H2SO4(浓)═NaHSO4+HCl↑ | ||
| C. | C+2H2SO4(浓)═2SO2↑+CO2↑+2H2O | D. | H2SO4+Na2SO3═Na2SO4+H2O+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
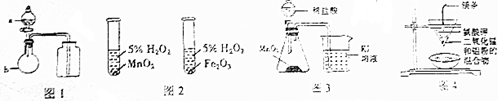
| A. | 用图1所示装置进行浓硫酸与亚硫酸钠的反应制取并收集SO2 | |
| B. | 用图2所示装置进行研究不同催化剂对反应速率的影响 | |
| C. | 用图3所示装置比较MnO2、Cl2、I2的氧化性 | |
| D. | 用图4所示装置可以制取金属锰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁片置于硫酸铜溶液中有铜析出 | |
| B. | 铁、铜和氯气反应分别生成FeCl3和CuCl2 | |
| C. | 足量的铁粉和铜粉与浓硫酸反应生成FeSO4和CuSO4 | |
| D. | 铜片置于FeCl3溶液中铜片逐渐溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | Na2CO3溶液中通入少量CO2:CO32-+CO2+H2O═2HCO3- | |
| C. | 金属Na与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
(1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
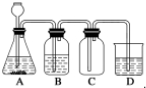
| A. | A 中可用分液漏斗代替长颈漏斗 | |
| B. | A 中缺少加热装置 | |
| C. | B 中盛放的NaOH 溶液可以净化Cl2 | |
| D. | D 中盛放的NaOH 溶液可以吸收尾气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com