
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂也不是还原剂 |
科目:高中化学 来源: 题型:解答题
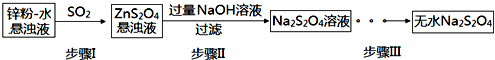
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na放置在空气中生成淡黄色的Na2O2固体 | |
| B. | Fe在O2中燃烧产物可用于制红色涂料 | |
| C. | Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到 | |
| D. | FeCl2溶液中滴加氨水至过量,加热蒸干溶液,最后灼烧可得到Fe2O3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO42-、MnO4- | ||
| C. | Cl-、SO32-、Fe2+、H+ | D. | Na+、H+、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
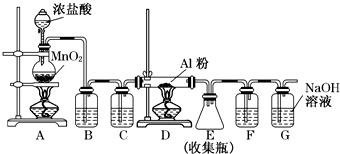
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:填空题
某反应的△H=+100kJ·mol-1,以下有关该反应的叙述正确是_________
①正反应活化能小于100kJ·mol-1
②逆反应活化能一定小于100kJ·mol-1
③正反应活化能不小于100kJ·mol-1
④正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 麻黄碱属于非处方药 | B. | 感冒时服用适量阿司匹林 | ||
| C. | 冰毒和海洛因不是毒品 | D. | 大部分药物都没有毒副作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2S除去废水中的Hg2+:Hg2++S2-═HgS↓ | |
| B. | Na在氧气中燃烧产生淡黄色固体:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| C. | 将NO2通入水中,生成硝酸:3NO2+H2O═2H++2NO3-+NO | |
| D. | Al与NaOH水溶液反应产生气体:Al+OH-+2H2O═Al(OH)3↓+2H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com