
【题目】催化剂在现代化学工业中占有极其重要的地位,主要涉及过渡元素及其化合物、硅、铝化合物等。中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。
(1)硅、碳位于同一主族,用“>”“<”或“=”填空:
性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
项目 | ①Si__________C | ②C_________Si | ③CO2______SiO2 | ④H-Si_______H-C |
(2)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有_____________(任写一种);1mol[Fe(CN)6]3-中含____________mol σ键。
(3)已知:反应2CH4![]() CH2=CH2+2H2,碳原子的杂化类型转化过程为___________;
CH2=CH2+2H2,碳原子的杂化类型转化过程为___________;
(4)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________方法区分晶体、准晶体和非晶体。
(5)基态F原子的价层电子排布图为___________。
(6)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为____________。
(7)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF的熔点比CuCl的高,原因是____________________________________________。
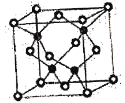
②已知NA为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数a=__________nm(列出计算式)。
【答案】> > < < N2(或CO等) 12 sp3转化成sp2 X射线衍射 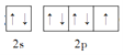 V形 CuCl为分子晶体,CuF为离子晶体
V形 CuCl为分子晶体,CuF为离子晶体 ![]() ×107
×107
【解析】
(1)①Si原子电子层数为3,C原子电子层数为2,所以半径Si>C;
②Si原子电子层数为3,C原子电子层数为2,所以C原子的原子核对核外电子的吸引能力更强,第一电离能更大;
③二氧化硅为原子晶体,二氧化碳为分子晶体,所以熔点:CO2>SiO2;
④Si原子半径更大,所以键能H-Si<H-C;
(2)原子总数相同,价电子总数也相同的分子或离子互为等电子体,CN-的原子数为2,价电子数为10,用N原子替换C原子与1个单位负电荷,或者用O原子替换N原子与1个单位负电荷,得到与CN-互为等电子体的分子为:N2或CO等;[Fe(CN)6]3-中Fe3+与CN-形成6个配位键,CN-中有1个σ键,故[Fe(CN)6]3-中共有12个σ键,1mol[Fe(CN)6]3-中含12molσ键;
(3)CH4为正四面体结构,C原子采取sp3杂化,CH2=CH2为平面结构,C原子采取sp2杂化,碳原子的杂化类型转化过程为:sp3杂化转化为sp2杂化;
(4)可通过X射线衍射实验方法区分晶体、准晶体和非晶体;
(5)F为9号原子,所以基态F原子的价层电子为2s22p5,排布图为 ;
;
(6)该离子中心原子价层电子对数为![]() =4,含有2对孤电子对,所以空间构型为V形;
=4,含有2对孤电子对,所以空间构型为V形;
(7)①根据CuCl熔化时几乎不导电可知其为分子晶体,熔点较低,而CuF为离子晶体,熔点较高;
②根据均摊法晶胞中F-个数为4,化学式为CuF,所以Cu+个数也为4,则晶胞的质量m=![]() g,晶胞的体积为a3nm3,晶胞密度为7.1g·cm-3=7.1×10-21 g·nm-3
g,晶胞的体积为a3nm3,晶胞密度为7.1g·cm-3=7.1×10-21 g·nm-3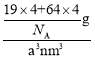 ,解得a=
,解得a=![]() ×107nm。
×107nm。


科目:高中化学 来源: 题型:
【题目】氰(CN)2、硫氰(SCN)2等称为拟卤素,它们与卤素单质性质相似,它们的阴离子也与卤素阴离子性质相似。例如:2Fe+3(SCN)2==2Fe(SCN)3、Ag++CN-== AgCN↓(白)。拟卤素形成的无氧酸和含氧酸一般比氢卤酸和次卤酸弱,阴离子的还原性一般比Br-强。下列反应中,不正确的是( )
A. 2CN-+Cl2= 2Cl-+(CN)2
B. (CN)2+2OH-=CN-+CNO-+H2O
C. (SCN)2+H2O = 2H++SCN-+SCNO-
D. MnO2+4HSCN(浓)![]() (SCN)2↑+Mn(SCN)2+2H2O
(SCN)2↑+Mn(SCN)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式为
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH为( )
A. -488.3 kJ·mol-1 B. -191 kJ·mol-1
C. -476.8 kJ·mol-1 D. -1 549.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期,李兰娟院士通过体外细胞实验发现抗病毒药物阿比多尔(H)能有效抑制冠状病毒,同时能显著抑制病毒对细胞的病变效应。合成阿比多尔的一条路线为:
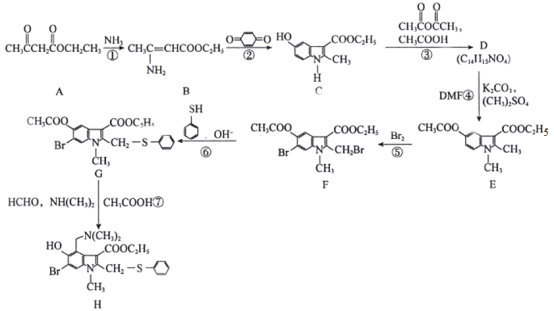
已知: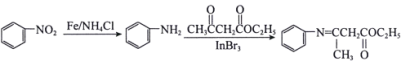 。
。
回答下列问题:
(1)阿比多尔分子中的含氧官能团为__________、____________,D的结构简式为______________。
(2)反应②的化学方程式为_______________;反应③的作用是_______________;反应⑤的类型为________________。
(3)A的同分异构体中,能发生银镜反应且能与碳酸氢钠溶液反应放出气体的有______种(不考虑立体异构)。
(4)以下为中间体D的另一条合成路线:
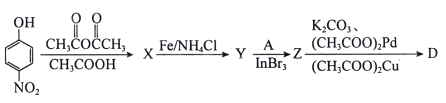
其中X、Y、Z的结构简式分别为_________、__________、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 mol·L-1 NaOH溶液滴定10 mL 0.100 mol·L-1 H3PO4溶液,曲线如图所示。下列说法正确的是
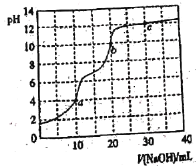
A.滴定终点a可选择酚酞作指示剂
B.c点溶液中c(Na+)>3c(PO43-)+2c(HPO42-)+c(H2PO4-)
C.b点溶液中c(HPO42-)>c(PO43-)>c(H2PO4-)
D.a、b、c三点中水的电离程度最小的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液VL,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗amolH2SO4、bmolAgNO3。则原混合溶液中的c(Na+)为( )
A. ![]() mol/LB.
mol/LB. ![]() mol/LC.
mol/LC. ![]() mol/LD.
mol/LD. ![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 石油裂解气可以使溴水褪色,也可以使高锰酸钾溶液褪色
B. 可以用新制的氢氧化铜检验乙醇中是否含有乙醛
C. 正丙醇(CH3CH2CH2OH)和钠反应要比水和钠反应剧烈
D. CH2=CHCH3+Cl2 ![]() CH2=CHCH2 Cl+ HCl属于取代反应
CH2=CHCH2 Cl+ HCl属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制氯气的尾气处理用_____溶液吸收,其化学反应方程式为_____。
(2)向AlCl3溶液中逐滴加入NaOH溶液,现象是先产生白色沉淀,其反应的离子方程式为_____,后白色沉淀又溶解消失,其反应的离子方程式为_____。
(3)在含有0.2mol的硫酸和0.2mol的硝酸的混合溶液200mL中,加入19.2g铜粉,产生的气体成分为_____(填NO或H2),你所选气体在标准状况下的体积为_____L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HClO4、H2SO4、HNO3和HCl都是强酸,它们的酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
下列说法中不正确的是( )
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中HClO4是这四种酸中最强的酸
C.在冰醋酸中H2SO4的电离方程式为H2SO4===2H++SO![]()
D.水不能区分这四种酸的强弱,但冰醋酸可以区分这四种酸的强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com