
下列表中对于相关物质的分类全部正确的一组是
编号 | 纯净物 | 混合物 | 弱电解质 | 非电解质 |
A | 明矾 | 蔗糖 | NaHCO3 | CO2 |
B | 天然橡胶 | 石膏 | SO2 | CH3CH2OH |
C | 冰 | 王水 | H2SiO3 | Cl2 |
D | 胆矾 | 玻璃 | H2CO3 | NH3 |
科目:高中化学 来源:2016届福建省高三上学期10月第一次月考化学试卷(解析版) 题型:填空题
新材料和新能源的开发和利用越来越成为科学家研究的方向。
典例一、用电弧法合成的储氢纳米常伴有大量的碳纳米顺粒(杂质),这种颗粒可用氧化气化法提纯,其反应式为:
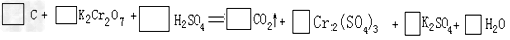
(1)完成配平上述反应的化学方程式:
(2)反应的氧化剂是__________,氧化产物是____________
(3)H2SO4在上述反应中表现出来的性质是________(填选项编号)(多选倒扣分)
A、酸性 B、氧化性 C、吸水性 D、脱水性
(4)上述反应中若产生0.2molCO2气体,则转移电子的物质的量是________mol
典例二、溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入 ,将其中的Br - 氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为 。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中, 显正电性。BrCl与水发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列反应的能量变化与其它三个不相同的是
A.铝粉与氧化铁的反应
B.氯化铵与消石灰的反应
C.锌片与稀硫酸反应
D.钠与冷水反应
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
美国研究人员将CO和O附着在一种钉催化剂表面,用激光脉冲将其加热到2000 K,成功观察到CO与O形成化学键生成CO2的全过程。下列说法不正确的是

A.CO2属于酸性氧化物
B.CO与O形成化学键的过程中放出能量
C.钌催化剂可以改变该反应的焓变
D.CO与O形成化学键的过程中有电子转移
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期10月月考化学试卷(解析版) 题型:选择题
某固体物质A在一定条件下受热分解产物都是气体,有关的化学方程式为:2A=B↑+2C↑+2D↑。若生成的混合气体对氘气的相对密度为d,则A的相对分子质量为
A.2d B.2.5d C.5d D.10d
查看答案和解析>>
科目:高中化学 来源:2016届湖南省浏阳市高三上学期第二次月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.Fe3O4溶于足量稀HNO3中:Fe3O4+8H+===Fe2++2Fe3++4H2O
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-===BaCO3↓+H2O
C.将过量的SO2通入Ca(ClO)2溶液中: SO2+ClO-+H2O===HClO+ HSO3-
D.将0.2 mol·L-1 NH4Al(SO4)2溶液与0.3 mol·L-1 Ba(OH)2溶液等体积
混合:2Al3++3SO42-+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期二次模拟测试理综化学试卷(解析版) 题型:填空题
元素周期表的用途广泛。
(1)用“>”或“<”填空:
离子半径 | 非金属性 | 熔点 | 沸点 |
K+_____S2- | N____O | 金刚石_____晶体硅 | HF____HCl |
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液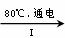 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
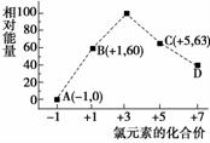
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期第一次月考化学试卷(解析版) 题型:填空题
(10分)已知反应:Fe(s)+CO2(g)  FeO(s)+CO(g)?H=akJ·mol?1
FeO(s)+CO(g)?H=akJ·mol?1
测得在不同温度下,该反应的平衡常数K值随温度的变化如下表所示:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)该反应的化学平衡常数表达式为 ,若在500℃2L密闭容器中进行该反应,CO2起始量为4mol,5min后达到平衡状态,则v(CO)为 。
(2)若在700℃时该反应达到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号,下同)。不能增大化学反应速率的有 。
A.缩小反应容器的体积
B.通入适量CO2
C.加入适量铁
D.升高温度到900℃
E.使用合适的催化剂
(3)下列图像符合该反应的是 (填序号)(图中v代表速率、ω代表混合物中CO的含量,T代表温度)。
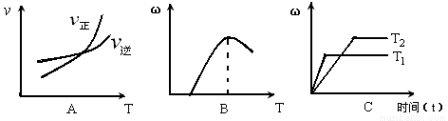
查看答案和解析>>
科目:高中化学 来源:2016届山西省校高三上学期阶段性考试化学试卷(解析版) 题型:填空题
现有①H2SO4 ②酒精 ③液氨 ④纯碱固体 ⑤熔融的氢氧化钠 ⑥水银 ⑦三氧化硫 ⑧澄清石灰水 ⑨氯化钠溶液 ⑩CaCO3固体,其中属于盐的是(填序号,下同)_________, 属于酸性氧化物的是_________,能导电的是_____________,属于电解质的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com