
| A. | 1 mol FeCl3水解生成的 Fe(OH)3胶粒数为 lNA | |
| B. | 将 lmol Cl2通人水中,HC1O、Cl、C1O 粒子数之和为 2NA | |
| C. | 1 mol Fe 溶于过量硝酸,电子转移数为 2NA | |
| D. | 10℃时,lL pH=1.0 的 H2SO4溶液中含 H+为 0.1NA |
分析 A.氢氧化铁胶粒为氢氧化铁的聚集体;
B.氯气溶于水,只有部分氯气参与反应;
C.硝酸过量,反应生成硝酸铁,1mol铁完全反应失去3mol电子;
D.pH=1.0的溶液中氢离子浓度为0.1mol/L,根据n=cV计算出氢离子的物质的量,然后计算出含有氢离子的数目.
解答 解:A.由于 Fe(OH)3胶粒为 Fe(OH)3的聚集体,则无法计算氢氧化铁胶粒的数目,故A错误;
B.将 lmol Cl2通入水中,由于溶液中含有氯气,则HC1O、Cl-、C1O- 粒子的物质的量之和小于2mol,粒子数之和为小于2NA,故B错误;
C.1mol Fe溶于过量硝酸,Fe完全转化成铁离子,失去电子的物质的量为3mol,则电子转移数为3NA,故C错误;
D.pH=1.0 的 H2SO4溶液中氢离子浓度为0.1mol/L,该溶液中含有氢离子的物质的量为:0.1mol/L×1L=0.1mol,含H+为0.1NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,B为易错点,注意只有部分氯气与水反应,试题培养了学生的分析能力及化学计算能力.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢能源的优点是热值高、无污染 | |
| B. | 与铜质水龙头连接处的铁质水管易发生锈蚀 | |
| C. | 放在冰箱电的食品保存时间较长,与温度对反应速率的影响有关 | |
| D. | 铅蓄电池放电时,电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg,Fe | B. | Zn,Ag | C. | Fe,Zn | D. | Mg,Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z 为 0.4mol•L-1 | B. | X 为 0.2 mol•L-1 | ||
| C. | Y 为 0.4 mol•L-1 | D. | Z 为 0.3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
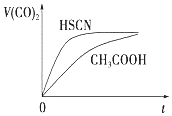 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | HSCN | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | Ka1=4.3×10-1Ka2=5.6×10-1 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中含有1mol的Na2SO4 | |
| B. | 从1L溶液中取出500 mL后,剩余溶液的浓度变为0.5mol/L | |
| C. | 1mol的Na2SO4 溶于1L水 | |
| D. | 1L溶液中含有142 g Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 10% | C. | 20% | D. | 24% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
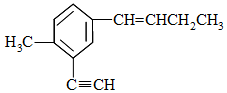
| A. | 与乙苯不互为同系物 | |
| B. | 分子中共直线的碳原子最多有4个 | |
| C. | 分子中共平面的原子最多有20个 | |
| D. | 与其互为同分异构体且萘环上只有一个侧链的共有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com