
| A. | 溶液中加入稀HNO3后,再加AgNO3溶液有黄色沉淀生成,则溶液中一定含Br- | |
| B. | 溶液中加入BaCl2有白色沉淀,再加入稀硝酸沉淀不溶解,则溶液中一定含SO42- | |
| C. | 溶液中加入NaOH溶液,加热后能产生使湿润的红色石蕊试纸变蓝的气体,则溶液中一定含NH4+ | |
| D. | 进行某溶液的焰色反应时,观察火焰呈黄色,则溶液中一定不存在K+ |
分析 A、溴化银沉淀是浅黄色的不溶于硝酸的物质,溴离子具有还原性,能被硝酸氧化;
B、液中加入BaCl2有白色沉淀,再加入稀硝酸沉淀不溶解,沉淀可以是氯化银或是硫酸钡;
C、铵根离子可以和氢氧化钠加热反应生成氨气;
D、钠元素的焰色反应显示黄色,钾元素的焰色反应只有透过钴玻璃才能看出是紫色.
解答 解:A、溶液中加入AgNO3溶液有淡黄色沉淀生成,稀HNO3后,再产生不溶解,则溶液中一定含Br-,故A错误;
B、溶液中加入BaCl2有白色沉淀,再加入稀硝酸沉淀不溶解,则溶液中一定含硫酸根或是氯离子中的至少一种,故B错误;
C、铵根离子可以和氢氧化钠加热反应生成氨气,氨气显示碱性,使湿润的红色石蕊试纸变蓝,故C正确;
D、进行某溶液的焰色反应时,观察火焰呈黄色,则溶液中一定存在钠离子,不能确定是否存在钾离子,故D错误.
故选C.
点评 本题考查物质的检验、鉴别实验方案的设计,题目难度中等,解答本题的关键是把握有关反应的现象以及离子的检验方法.


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO${\;}_{3}^{2-}$ NO${\;}_{3}^{-}$ SO${\;}_{4}^{2-}$ SiO${\;}_{3}^{2-}$ |
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
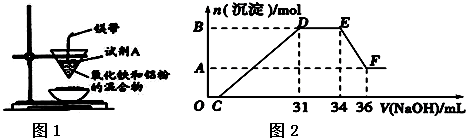
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2 | B. | NO | C. | N2O5 | D. | NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱---剧毒品 | B. | 汽油---易燃品 | C. | 浓硫酸---腐蚀品 | D. | 酒精---易燃品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=△H1+2△H2 | B. | △H3=△H1+△H2 | C. | △H3=△H1-2△H2 | D. | △H3=△H1-△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤②③①④ | B. | ④①③②⑤ | C. | ③②①⑤④ | D. | ③②④①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com