
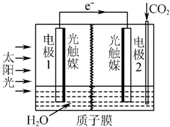
 利用人工光合作用合成甲酸的原理为2CO2+2H2O
利用人工光合作用合成甲酸的原理为2CO2+2H2O| 太阳能 |
| 光触媒 |
| A、该装置将太阳能转化为化学能和电能 |
| B、电极1周围pH增大 |
| C、电极2上发生的反应为:CO2+2H++2e-═HCOOH |
| D、H+由电极1室经过质子膜流向电极2室 |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
| A、将少量SO2气体通入NaClO溶液中SO2+2ClO-+H2O═SO32-+2HClO |
| B、苯酚钠溶液中通入少量的二氧化碳气体C6H5O-+CO2+H2O═C6H5OH+HCO3- |
| C、足量的溴化亚铁溶液和少量的氯气反应2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| D、向氯化铝溶液中加入过量的氨水Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH皆等于3 的两种溶液都稀释100倍后,pH都为5 |
| B、10mL 0.02mol/L HCl溶液与10mL 0.02mol/L Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7 |
| C、在0.1mol/L某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
| D、室温下,在一定量稀氨水中逐滴滴入稀盐酸,对于所得溶液中离子浓度大小关系可能是:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L Na2CO3溶液中的Na+数目为2NA |
| B、电解Na2CO3饱和溶液,若生成2NA个H2,一定生成NA个O2 |
| C、常温常压下,46g NO2的原子数为3NA |
| D、1mol Na2O2与H2O完全反应时转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、有机物X与Y互为同系物 |
| B、有机物Y与阿维A酯均能与NaOH溶液反应 |
| C、一定条件下1mol阿维A酯能与4mol H2发生加成反应 |
| D、X中有6种化学环境不同的氢原子,Y中有1个手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
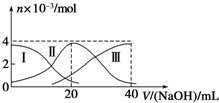 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )| A、当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
| B、等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水大 |
| C、NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) |
| D、向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性:H3AsO4>H2SO4>H3PO4 |
| B、微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C、热稳定性:HF>HCl>HBr>HI |
| D、熔点:SiO2>NaCl>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠的焰色反应(铂丝、氯化钠溶液、稀盐酸) |
| B、蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液) |
| C、硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体) |
| D、肥皂的制取(蒸发皿、玻璃棒、甘油) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度为0.1mol/L NaClO溶液和0.1mol/L CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 配制FeCl2溶液时,先将FeCl2溶于适量稀盐再用蒸馏水稀释,最后在试剂瓶中加入少量铜粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com