
(1)用双线桥表示铜与稀硝酸反应电子转移的方向和数目_____________
________________________________________________________________________。
(2)该反应的氧化剂是__________(填化学式),氧化产物与还原产物的物质的量之比为____________。
(3)已知实验室中只有16 mol·L-1的浓硝酸,若要配制100 mL 0.8 mol·L-1的稀硝酸所需浓硝酸的体积为________mL。定容时由于俯视刻度,则对浓度产生的影响为__________(填“偏高”、“偏低”或“无影响”)。
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.25 ℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA
B.1.2 g C60和石墨的混合物中,含有的碳原子数目为0.1NA
C.2.24 L N2和NH3的混合气体中,含有的共用电子对数目为0.3NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的检验方法正确的是 ( )。
A.向某无色溶液中滴加氯化钡溶液,产生白色沉淀,再加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO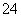
B.某溶液能使淀粉碘化钾溶液变蓝,则该溶液一定为氯水或者溴水
C.向某白色固体粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原固体粉末中一定含有CO 或HCO
或HCO
D.将某白色固体粉末与氢氧化钠浓溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,证明原固体中一定含有NH
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO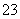
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO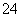
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH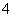
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有a mol AlCl3的溶液中加入含b mol KOH的溶液,生成沉淀的物质的量可能是( )
①a mol ②b mol ③ mol ④
mol ④ mol ⑤0 mol ⑥(4a-b)mol
mol ⑤0 mol ⑥(4a-b)mol
A.①②④⑤⑥ B.①④⑤⑥ C.①②③⑤⑥ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关因果关系的描述正确的是
A.因为盐酸的酸性强于氢硫酸,所以氯元素的非金属性强于硫
B.因为醋酸电离吸热,所以用NaOH溶液中和等体积等浓度的醋酸和盐酸,前者放出热量少
C.因为KCl的溶解度随温度的降低而减小,所以降低温度KCl溶液的质量分数一定会减小
D.因为C3H8(g)+5O2(g)=3CO2(g)+4H2O(1)需要加热方能发生,所以该反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列叙述正确的是
A.标准状况下,22.4 L氦气中含有的电子数为2NA
B.11g的2H218O分子中含NA个中子
C.1molNH4+离子所含的质子总数为10NA
D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为____________________;加入硅、锰和铝的目的是________________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是______________________。
(4)炼铁和炼钢生产中,尾气中均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
(1)该电池的负极材料是________。电池工作时,电子流向________(填“正极”或“负极”)。
(2)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________。欲除去Cu2+,最好选用下列试剂中的________(填选项字母)。
A.NaOH B.Zn
C.Fe D.NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com