
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) ![]() 2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是( )
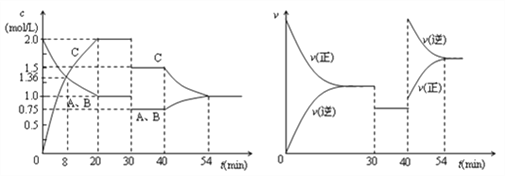
A. 前20min B的平均反应速率为0.05mol·L-1·min-1
B. 8 min时表示正反应速率等于逆反应速率
C. 反应方程式中的x=1,30 min时表示增大压强
D. 40 min时改变的条件是升高温度,且正反应为吸热反应
【答案】A
【解析】
A.根据图像可知,前20min B的物质的量浓度由2.0mol/L降至1.0mol/L,则B的平均反应速率为(2.0mol/L-1.0mol/L)÷20min=0.05 mol·L-1·min-1,A项正确;B.8min时,A、B、C三种物质的浓度相等,但随后A、B的浓度减小,C的浓度增大,说明此时正反应速率大于逆反应速率,B项错误;C.反应方程式中的x=1,该反应为前后气体系数和不变的可逆反应,若增大压强,平衡不移动,三种物质的浓度都同等程度的增大,与所给图像变化不符,C项错误;D.40min时正逆反应速率均增大,且逆反应速率大,平衡逆向移动,升高温度,平衡向吸热反应方向移动,则该反应正反应为放热反应,D项错误。答案选A。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】0.3L 1mol·L-1FeCl3溶液与0.2L 1mol·L-1KCl溶液中,Cl-浓度比是
A. 9:2 B. 3:2 C. 3:1 D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将氧化铝加入水中得到氢氧化铝
B. 因为Al2O3是金属氧化物,所以它是碱性氧化物
C. Al2O3不能跟所有的酸、碱溶液反应
D. 制备Al(OH)3悬浊液时,向1mol·L-1AlCl3溶液中加过量的6mol·L-1NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯(CH2==CH2)和环丙烷(CH2H2CCH2)比较的说法中,正确的是( )
A. 它们都为不饱和烃 B. 它们属于同系物
C. 互为同分异构体 D. 碳、氢元素的质量比相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列放热反应的说法中正确的是( )
A. 只要是释放热量的变化就是放热反应
B. 只要是释放热量的化学变化就是放热反应
C. 不需要加热就能反应的化学反应就是放热反应
D. 反应物的总能量小于生成物的总能量的化学反应就是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯和乙烷比较的说法中,正确的是( )
A. 它们都属于饱和链烃
B. 它们组成元素的质量比相同
C. 相同质量完全燃烧时,生成二氧化碳的质量相同
D. 相同物质的量完全燃烧时,生成二氧化碳的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学设计了如图装置制取溴苯和溴乙烷:

已知:乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
溶解性(本身均可作溶剂) | 沸点(℃) | 密度(g/mL) | |
乙醇 | 与水互溶,易溶于有机溶剂 | 78.5 | 0.8 |
溴乙烷 | 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
请回答下列问题:
(1)B中发生反应生成目标产物的化学方程式为___________。
(2)根据实验目的,选择合适的实验步骤:①→____________。
①组装好装置,_________________(填写实验操作名称);
②将A装置中的纯铁丝小心向下插入苯和液溴的混合液中;
③点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10分钟;
④向烧瓶中加入一定量苯和液溴,向锥形瓶中加入无水乙醇至稍高于进气导管口处,向U形管中加入蒸馏水封住管底,向水槽中加人冰水。
(3)简述实验中用纯铁丝代替铁粉的优点:_________________。
(4)反应完毕后,U形管内的现象是_________;分离溴乙烷时所需的玻璃仪器是___________。
(5)假设最初取用的无水乙醇是71.9 mL,最后得到的纯净的溴乙烷是66.2 mL,则溴乙烷的产率为______________(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用乙醛生产PTT(聚酯)和化合物M 的某种合成路线如下:

回答下列问题:
(1)A中官能团名称为______.
(2)B生成C的反应类型为_______。
(3)C的结构简式为_______,D化学名称是_______。
(4)由D生成PTT的化学方程式为____________________。
(5)芳香化合物W是M的同分异构体,它的溶液滴入FeCl3溶液显紫色,W共有______种(不含立体结构),其中核磁共振氢谱为四组峰的结构简式为_________。
(6)参照上述合成路线,以乙醇和1,3-丁二烯为原料(无机试剂任选),设计制备合成 路线___________________。
路线___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)﹣空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )

A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 在Mg﹣空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
C. M﹣空气电池放电过程的正极反应式:正极反应式为O2+2H2O+4e﹣=4OH﹣
D. 比较Mg、Al、Zn三种金属﹣空气电池,Mg﹣空气电池的理论比能量最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com