
���� ��1��CeO2��ϡ�����H2O2�������¿�����Ce3+��CeԪ�صĻ��ϼ���+4�۽���Ϊ+3�ۣ��������غ㡢����غ�͵����غ�ĽǶ���ƽ����ʽ��
��2����Ӧ��CrԪ�ػ��ϼ���+6�۽��͵�+3�ۣ�SԪ�ػ��ϼ���+4�����ߵ�+6�ۣ�����С������Ϊ12���ɵ����غ��ԭ���غ㡢����غ��֪��ƽ��
��3��SnCl2����Һ�з���ˮ������Sn��OH��Cl��
��� �⣺��1��CeO2��ϡ�����H2O2�������¿�����Ce3+��CeԪ�صĻ��ϼ���+4�۽���Ϊ+3�ۣ���CeO2�ڷ�Ӧ������������
��Ӧ��CrԪ�ػ��ϼ���+6�۽��͵�+3�ۣ�OԪ�ػ��ϼ���-1�����ߵ�0�ۣ��ɵ����غ��ԭ���غ㡢����غ��֪��ƽ������ӷ���ʽΪ��Cr2O72-+3H2O2+8H+�T2Cr3++3O2��+4H20��
�ʴ�Ϊ��������Cr2O72-+3H2O2+8H+�T2Cr3++3O2��+4H20��
��2����Ӧ��CrԪ�ػ��ϼ���+6�۽��͵�+3�ۣ�SԪ�ػ��ϼ���+4�����ߵ�+6�ۣ�����С������Ϊ12���ɵ����غ��ԭ���غ㡢����غ��֪��ƽ������ӷ���ʽΪ��
Cr2O72-+3SO32-+8H+�T2Cr3++3SO42-+4H20��
�ʴ�Ϊ��Cr2O72-+3SO32-+8H+�T2Cr3++3SO42-+4H20��
��3��SnCl2����Һ�з���ˮ������Sn��OH��Cl���䷴Ӧ����ʽΪ��SnCl2+H20?Sn��OH��Cl+HCl��
�ʴ�Ϊ��SnCl2+H20?Sn��OH��Cl+HCl��
���� ���⿼��������ԭ��Ӧ��������ѧ���ķ��������Ŀ��飬��ȷ��Ӧ��Ԫ�صĻ��ϼ۱仯�ǽ��Ĺؼ���ע������غ��ԭ���غ��Ӧ�ã���Ŀ�Ѷ��еȣ�


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ٵμ�AgNO3��Һ���۲��Ƿ���AgI�������� | |
| B�� | ����CC14�۲��²�Һ����ɫ | |
| C�� | ����CC14��ȡ�ϲ���Һ���μ�AgNO3��Һ���۲��Ƿ���AgCl�������� | |
| D�� | ����CC14��ȡ�ϲ���Һ���μ�KSCN��Һ���۲��Ƿ���Ѫ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ŀ | ���ȱ� | β�� | ��ȷ������ | ��ʧ���� |
| ����ʧ����kg/t�� | 13 | 24.9 | 51.3 | 89.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɢϵ�з�ɢ�����ӵĴ�С��Fe��OH��3����Һ��Fe��OH��3���壼FeCl3��Һ | |
| B�� | ��ɫ��Ӧ������ȼ��ʱ������ֵ���ɫ�仯�����ڻ�ѧ�仯 | |
| C�� | ��ʯ������ʳƷ������ | |
| D�� | ����ˮ���������Խ������ˮ��ӦΣ��������������������ʹ��ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�س��ʱ��﮼������Դ�ĸ������� | |
| B�� | �õ�طŵ�ʱ��Li+���ƶ� | |
| C�� | �õ�س��ʱ�����ķ�ӦΪLixV2O4-xe-=V2O4+xLi+ | |
| D�� | ���ŵ�ʱת�� 0.2 mol ���ӣ�������� 1.4x g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 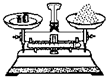 ��ȡ�������� | B�� |  Ũ����ϡ�� | C�� | 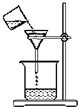 ������Һ | D�� | 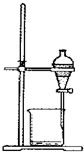 ��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L������������ΪNA | |
| B�� | 1mol������������Ϊ10NA | |
| C�� | ���³�ѹ�£�5.6 g��ϩ�붡ϩ�Ļ�����к��е���ԭ����ĿΪ0.8NA | |
| D�� | 12 g���ʯ�к���C-C���ĸ���Ϊ4NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com