
 ”的同分异构体有( )
”的同分异构体有( )| A. | 7种 | B. | 9种 | C. | 11种 | D. | 13种 |
分析 该有机物相对分子质量为17×6=102,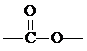
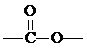
(1)C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被-COOH夺取,即由丁基与-COOH构成,其同分异构体数目与丁基异构数目相等;
(2)分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行书写判断.
解答 解:该有机物相对分子质量为17×6=102,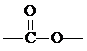
(1)C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被-COOH夺取,即由丁基与-COOH构成,其同分异构体数目与丁基异构数目相等,-C4H9有4种结构,分别为:CH3-CH2-CH2-CH2-、CH3-CH2-CH(CH3)-、(CH3)2CH-CH2-、(CH3)3C-,即有4种羧酸;
(2)若该有机物为酯,分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行书写判断:
若为甲酸和丁醇酯化,丁醇有4种,形成的酯有四个:
HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2个:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1个:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2个:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3.
故有9种.
所以分子中含有“ ”的同分异构体共有13种,
”的同分异构体共有13种,
故选D.
点评 本题考查同分异构体数目的求算,题目难度中等,可以根据有机物结构利用换元法进行解答,注意掌握同分异构体的概念及书写原则,试题培养了学生灵活应用基础知识的能力.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4在酸性溶液中不稳定,与水反应生成Fe3+和O2,离子方程式为:4FeO42-+10H2O+4Fe3+=20OH-+3O2↑ | |
| B. | 工业上可用FeCl3、NaOH、NaClO三种物质反应制得NaFeO4离子方程式为:2Fe3++10OH-+3ClO-=2FeO42-+3Cl-+5H2O | |
| C. | NaFeO4消毒杀菌时得到的Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++3H2O?Fe(OH)3+3H+ | |
| D. | 工业上可用铁做阳极,电解浓NaOH溶液的方法制Na2FeO4,阳极的电极反应为:Fe-6e-+8OH-=FeO42-+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使石蕊溶液呈红色的溶液:Fe2+、Na+、Ba2+、Cr2O72-可以大量共存 | |
| B. | 氢氧化钡溶液与等物质的量的稀硫酸混合,离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 50℃,pH=1的硫酸溶液中:c(H+)=0.1mol/L | |
| D. | 25℃,pH相同的NaOH、CH3COONa、Na2CO3、NaHCO3溶液的浓度c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H8O2属于酯的同分异构体 | B. | C5H10O2属于酸的同分异构体 | ||
| C. | 甲苯的一氯取代物 | D. | 化合物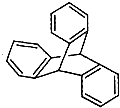 的一氯取代物 的一氯取代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| B. | 水电离出的c(H+)=1×10-14mol•L-1的溶液中:Ba2+、NO3-、K+、SO32- | |
| C. | 使苯酚显紫色的溶液中:NH4+、Na+、Cl-、SCN- | |
| D. | 使甲基橙变红的溶液中:Na+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com