
| A. | 含1mo1K0H的溶液与1mo1CO2完全反应后,溶液中c(K+)>c(HCO3- ) | |
| B. | 0.2mo1/LCH3COOH溶液与0.1mo1/LNaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| C. | 将100mL0.1mo1.L-1的醋酸稀释至pH=4:n(CH3COO-)+n(CH3COOH)=0.01mo1 | |
| D. | pH=5的NaHSO3溶液中:c(HSO3-)+c(SO32-)=c(Na+) |
分析 A.二者恰好反应生成KHCO3,钾离子不水解、碳酸氢根离子水解;
B.二者混合后溶液中溶质为等物质的量浓度的CH3COONa、CH3COOH,溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.pH=5的亚硫酸氢钠溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒判断.
解答 解:A.二者恰好反应生成KHCO3,钾离子不水解、碳酸氢根离子水解,所以存在c(K+)>c(HCO3- ),故A正确;
B.二者混合后溶液中溶质为等物质的量浓度的CH3COONa、CH3COOH,溶液中存在电荷守恒和物料守恒,
根据物料守恒有:c(CH3COO-)+c(CH3COOH)=2c(Na+),
根据电荷守恒有:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),
整理得:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),故B正确;
C.任何电解质溶液中都存在物料守恒,根据物料守恒n(CH3COO-)+n(CH3COOH)=0.1mol/L×0.1L=0.01mo1,故C正确;
D.pH=5的亚硫酸氢钠溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒得c(HSO3-)+2c(SO32-)=c(Na+),故D错误;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,把握物料守恒、电荷守恒是解本题关键,注意守恒思想的灵活运用,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷 | B. | 乙醇 | C. | 乙酸 | D. | 蔗糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,其与过量的NaOH溶液反应的化学方程式是
,其与过量的NaOH溶液反应的化学方程式是 +2NaOH→
+2NaOH→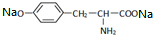 +2H2O.
+2H2O.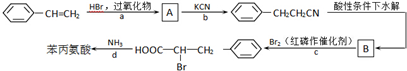
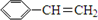 +HBr→
+HBr→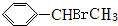 .
. +Br2$\stackrel{红磷}{→}$
+Br2$\stackrel{红磷}{→}$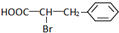 +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其他步骤正确,滴定达到终点时,俯视读数,测得c(H+)偏大 | |
| B. | 实验测得25℃时,HgI2的Ksp=4×10-9 | |
| C. | 一定温度下,向HgI2饱和溶液中加入少量Hg(NO3)2溶液,HgI2的Ksp减小 | |
| D. | 温度不变,在t时,向HgI2饱和溶液中加入少量浓KI溶液,离子浓度变化如图所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
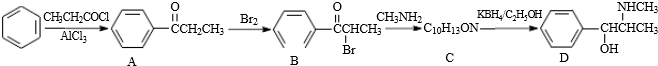
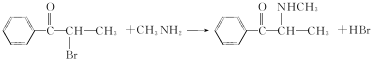 .C-D的反应类型为还原反应.
.C-D的反应类型为还原反应.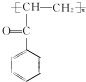
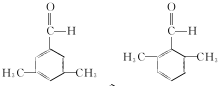 (写结构简式).
(写结构简式). 参照上述合成路线,设计一条由苯和乙酸为起始原料制备
参照上述合成路线,设计一条由苯和乙酸为起始原料制备 的合成路线:
的合成路线: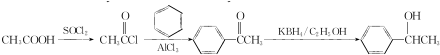 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com