
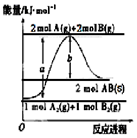
| A. | 该反应热△H=+(a-b)kJ•mol-1 | |
| B. | AB(g)═A(g)+B(g)△H=+b/2kJ•mol-1 | |
| C. | 断裂1 mol A-A键和1 mol B-B键,吸收a kJ能量 | |
| D. | 该反应在任何条件下都不可能自发进行 |
分析 A.由图可知,1molA2(g)、1molB2(g)的总能量小于2molAB(s)的总能量,为吸热反应;
B.互为逆反应的焓变数值相同,符号相反,且物质的量与热量成正比;
C.断裂化学键需要稀释能量;
D.△H-T△S<0的反应可自发进行.
解答 解:A.由图可知,1molA2(g)、1molB2(g)的总能量小于2molAB(s)的总能量,为吸热反应,则A2(g)+B2(g)═2AB(s)△H=+(a-b)kJ•mol-1,故A正确;
B.互为逆反应的焓变数值相同,符号相反,且物质的量与热量成正比,则AB(g)═A(g)+B(g)△H=-$\frac{(a-b)}{2}$kJ•mol-1,故B错误;
C.断裂化学键需要稀释能量,则断裂1 mol A-A键和1 mol B-B键,吸收a kJ能量,故C正确;
D.△H-T△S<0的反应可自发进行,△H>0,△S<0,则在任何条件下都不可能自发进行,故D正确;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、热化学方程式及反应进行方向的判断为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.


科目:高中化学 来源: 题型:实验题
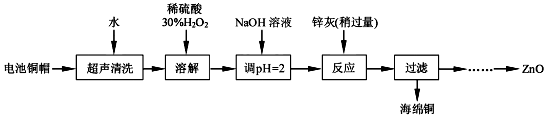
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 编号 | 起始时各物质的物质的量/mol | 达到平衡时体系的变化 | 平衡时NH3的体积分数 | ||
| N2 | H2 | NH3 | |||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ | W1 |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q kJ | W2 |
| A. | W1>W2,Q<23.15 | B. | W1=W2,Q=23.15 | C. | W1<W2,Q>23.15 | D. | W1=W2,Q<23.15 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
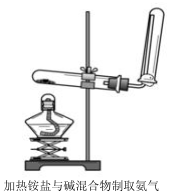 实验室一般采用如下装置制取氨气,按要求回答下列问题:
实验室一般采用如下装置制取氨气,按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 | |
| B. | 化石燃料在任何条件下都能充分燃烧 | |
| C. | 燃烧热或中和热是反应热的种类之一 | |
| D. | 弱酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=4 | |
| B. | 平衡时气体压强是原来压强的1.1倍 | |
| C. | A的平衡浓度是1.4 mol•L-1 | |
| D. | B的转化率是40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用A表示反应的速率为0.1 mol•L-1•s-1 | |
| B. | 用B表示反应速率为0.4 mol•L-1•s-1 | |
| C. | 3s时生成C的物质的量为1.2mol | |
| D. | 3s时B的浓度为0.6mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com