
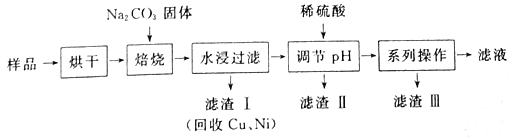
����Ŀ��ij��ҵ�������к���Cr(OH)3��Al2O3��CuO��NiO�����ʣ���ҵ��ͨ���������̻����������õĽ�������ȡNa2Cr2O7��
��֪��
����ˮ�������������Һ�д���Na2CrO4��NaAlO2������
�ڳ�ȥ����II����Һ�д��ڷ�Ӧ2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
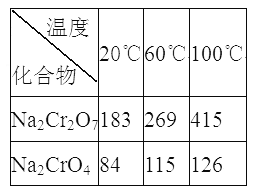
��Na2Cr2O7��Na2CrO4�ڲ�ͬ�¶��µ��ܽ�ȣ�g/100 g H2O)���±���
(1) ������������������NaAlO2��ѧ����ʽΪ_____________________��
(2)��������IIʱ,���������ϡ���������Һ��pH��ȥA1O2-����ϡ��������������������Ӧ�����ӷ���ʽΪ______________________��
(3) ��ϵ�в�����Ϊ����������ϡ���ᡢ_____����ȴ�ᾧ�����ˡ���������ϡ�����Ŀ����_____________������III����Ҫ�ɷ���_________(�ѧʽ)��
(4)��ҵ�ϻ���������ˮ���������������Һ�м�������ϡ���ᣬ��ʯī���缫��������������������ĵ缫��ӦʽΪ______________��
(5)����ͼ���ġ���Һ������Ȼ�в�����Na2Cr2O7��CrΪ�ؽ���Ԫ�أ����������߾���������У���Ժ�ˮ����ؽ�����Ⱦ��Ϊ�ⶨ����Һ���е�c(Na2Cr2O7)��ijʵ��С��ȡ����Һ��20mL��ˮϡ����250 mL����ȡϡ�ͺ����Һ25 mL����ƿ�У���c mol L-1��FeSO4��Һ����������ԭ�ζ������յ�ʱ����FeSO4��Һ���ΪV mL������Һ���е�c(Na2Cr2O7)=______mol��L-1��
���𰸡� A12O3+NaCO3![]() 2NaAlO2+CO2�� A1(OH)3+3H+==Al3++3H2O ����Ũ�� �ٽ���ѧƽ��2CrO42-+2H+
2NaAlO2+CO2�� A1(OH)3+3H+==Al3++3H2O ����Ũ�� �ٽ���ѧƽ��2CrO42-+2H+![]() Cr2O72-+H2O������Ӧ�����ƶ������������ɸ����Na2Cr2O7 Na2Cr2O7 Cr2O72-+14H++12e-==2Cr��+7H2O
Cr2O72-+H2O������Ӧ�����ƶ������������ɸ����Na2Cr2O7 Na2Cr2O7 Cr2O72-+14H++12e-==2Cr��+7H2O ![]()
���������Ժ���Cr(OH)3��Al2O3��ZnO��CuO��NiO�����ʵĵ������Ϊԭ�ϣ���ɺ����̼���ƺ������������շ�����Ӧ4Cr(OH)3+4Na2CO3+3O2![]() 4Na2CrO4+6H2O+4CO2��Al2O3+Na2CO3
4Na2CrO4+6H2O+4CO2��Al2O3+Na2CO3![]() Na2AlO3+CO2����ZnO++Na2CO3
Na2AlO3+CO2����ZnO++Na2CO3![]() Na2ZnO2+CO2����ˮ������˵õ�����CuO��NiO����ҺΪNa2CrO4��NaAlO2��Na2ZnO2�ȣ�������ҺpH����ZnO22-���Ӻ�ƫ��������ӣ����˵õ���ҺNa2CrO4�����������ữ�����ظ�������Һ��ͨ���ᴿ�õ��ظ����ơ�
Na2ZnO2+CO2����ˮ������˵õ�����CuO��NiO����ҺΪNa2CrO4��NaAlO2��Na2ZnO2�ȣ�������ҺpH����ZnO22-���Ӻ�ƫ��������ӣ����˵õ���ҺNa2CrO4�����������ữ�����ظ�������Һ��ͨ���ᴿ�õ��ظ����ơ�
(1) ������������������NaAlO2��ѧ����ʽΪAl2O3+Na2CO3![]() Na2AlO3+CO2�����ʴ�Ϊ��Al2O3+Na2CO3
Na2AlO3+CO2�����ʴ�Ϊ��Al2O3+Na2CO3![]() Na2AlO3+CO2����
Na2AlO3+CO2����
(2)���������������ԣ�������ϡ�����ܹ��ܽ����ɵ�����������������Ӧ�����ӷ���ʽΪA1(OH)3+3H+==Al3++3H2O���ʴ�Ϊ��A1(OH)3+3H+==Al3++3H2O��
(3)ˮ������Һ�д���Na2CrO4���������ᷢ��CrO42-+2H+Cr2O72-+H2O�����������ʹƽ��������Ӧ�����ƶ�������Һ����Ũ������ȴ�ᾧ�ɵõ������Na2Cr2O7���壬�ʴ�Ϊ������Ũ�����ٽ�ƽ��CrO42-+2H+Cr2O72-+H2O������Ӧ�����ƶ������������ɸ����Na2Cr2O7���壻Na2Cr2O7��
(4)���ɸ��ĵ缫������ԭ��Ӧ��Cr2O72-�õ���������Cr����Ӧ�ĵ�ⷽ��ʽΪCr2O72-+14H++12e-==2Cr��+7H2O���ʴ�Ϊ��Cr2O72-+14H++12e-==2Cr��+7H2O��
(5) V mL c mol L-1��FeSO4��FeSO4�����ʵ���ΪcV��10-3mol����Na2Cr2O7��Ӧ���������ӣ�ת�Ƶ���cV��10-3mol�����ݵ�ʧ�����غ㣬Na2Cr2O7ת��ΪCr3+ʱ�õ�cV��10-3mol���ӣ���n(Na2Cr2O7)= ![]() mol����c(Na2Cr2O7)=
mol����c(Na2Cr2O7)=  ��
��![]() =
=![]() mol/L���ʴ�Ϊ��
mol/L���ʴ�Ϊ�� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ����ijŨ�����Լ�ƿ�ı�ǩ���Ը��ݱ�ǩ�ϵ��й����ݻش��������⣺
����
����ʽ��H2SO4
��Է���������98
�ܶȣ�1.84g/mL
H2SO4������������98%
��1����Ũ������H2SO4�����ʵ���Ũ��Ϊ_________��
��2��ijѧ����������Ũ���������ˮ����100mL���ʵ���Ũ��Ϊ0.8 mol��L��1��ϡ���ᣬ��ѧ����Ҫ��ȡ_________mL����Ũ����������ơ�
��3��Ϊ���ƣ�2���е�ϡ���ᣬ������Ͳ���ձ�����ͷ�ι��⣬��ȱ�ٵIJ���������_________��
��4�������ƹ����У�����ʵ��������ܵ������Ƶ�������ҺŨ��ƫ�ߵ���_________������ţ���
a������ʱ���ӹ۲�
b�����ݺ���ҡ�ȡ����ú���Һ���½����ټ�����������ˮ
c��Ũ�������ձ��м�ˮϡ�ͺ�δ��ȴ��������ƿ��ת��
d������ƿδ���T����������Һ
e��������ƿת��ʱ��������Һ�彦����
f��δϴ��ϡ��Ũ������ձ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ 63%��Ũ HNO3 �����ܶ�Ϊ 1.4 g��mL -1������ 240 mL 0.50 mol��L-1 ϡ HNO3����ʵ�������У�
A.10 mL ��Ͳ B.50 mL ��Ͳ C.������ƽ D.������ E.100 mL ����ƿ F.250 mL ����ƿ G.500 mL ����ƿ H.��ͷ�ι� I.200mL �ձ�
��1����Ũ��������ʵ���Ũ��Ϊ_____mol��L -1��
��2��Ӧ��ȡ 63%��Ũ����_____mL��Ӧѡ��_____������������ĸ��ţ���
��3��ʵ��ʱ����ѡ�õ������� D��I��______������ţ���
��4�����ƹ����У����в�����ʹ���Ƶ�ϡ������ҺŨ��ƫ�ߵ��ǣ�����ţ�______��
����ȡŨ�������Ͳ������ˮϴ�� 2~3 �Σ�����ϴ��Һת������ƿ
������ƿʹ��ʱδ����
���ܽ��δ����ȴ����Һ
������ʱ��С������������ˮ�ε�ƿ��
�����ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[ѡ��5���л���ѧ����]��20�֣�
����6�֣�
��éȩ�� ������Ϊ�ϳ������ص��м��壬������éȩ��������ȷ����
������Ϊ�ϳ������ص��м��壬������éȩ��������ȷ����
A������ʽΪC10H18O B�����ܷ���������Ӧ
C����ʹ����KMnO4��Һ��ɫ D����������7�ֲ�ͬ��ѧ��������
����14�֣�
���Ѽ����˵��������ͬʱ��R1��O��R2��R1��R2����ͨ������Ϊ�����ѡ������ô���ˮ�ij��淽���Ʊ����ѣ����������ั���
R1��OH+ R2��OH ![]() R1��O��R2+ R1��O��R1+ R2��O��R2+H2O
R1��O��R2+ R1��O��R1+ R2��O��R2+H2O
һ����Williamson��Ӧ�Ʊ����ѣ�R1��X+ R2��ONa��R1��O��R2+NaX��ij�����о�С����ϳ�![]() ���һ��л��ѣ���������������·�߽��жԱȣ�
���һ��л��ѣ���������������·�߽��жԱȣ�
����![]()
������![]()
��![]()
��![]()
�ش��������⣺
��1��·��������Ҫ��������______________��______________��
��2��A�Ľṹ��ʽΪ______________��
��3��B���Ʊ�������Ӧע��İ�ȫ������______________��
��4����A��B�����һ��л��ѵķ�Ӧ����Ϊ______________��
��5���Ƚ������ϳ�·�ߵ���ȱ�㣺______________��
��6�����״���ͬ���칹���к��б����Ļ���________�֡�
��7��ijͬѧ�ø�Ϊ�����õļױ�������״��ϳ��һ��л��ѣ������·������д���ϳ�·��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ˮ��Ӧ������ˮú����������壩���䷴Ӧ����ʾ��ͼ��ͼ��ʾ������������ʾ��ͼ�ó��Ľ����У���ȷ����( )

A. ��Ӧǰ���Ԫ�صĻ��ϼ۾�����
B. ˮú���ijɷ���һ����̼������
C. �÷�Ӧ�к���Ԫ�صĻ�������3��
D. �÷�Ӧ�Ļ�ѧ����ʽ�м����ˮ�ļ�����֮��Ϊ1�U1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ��ÿ��ת��ͨ��һ����Ӧ��ʵ�ֵ��ǣ� ��
A. Al �� Al2O3�� Al(OH)3�� NaAlO2
B. N2�� NO�� NO2�� HNO3
C. Si �� SiO2�� H2SiO3�� Na2SiO3
D. S �� SO3�� H2SO4�� MgSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������۷����Ȼ�����Һ�У���ȫ��Ӧ��������Һ��Fe2+��Fe3+�����ʵ���Ũ��֮��Ϊ1��2�����ѷ�Ӧ��Fe3+��δ��Ӧ��Fe3+�����ʵ���֮��Ϊ�� ��
A��1��1 B��1��2 C��1��3 D��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������±��ṩ�IJ����������Dz���������ѡ����ʵ��װ�þ��ܴﵽ��Ӧʵ��Ŀ�ĵ���
ѡ�� | A | B | C | D |
ʵ��Ŀ�� | ��ȥKCl������MnO2 | ��10 mol��L-1��������100mL0.1 mol��L-1���� | �ú�������NH4Cl���ʵ�NaCl��Һ�Ʊ��Ȼ��ƾ��� | ����Ȳ�ķ���װ�� |
ʵ��������װ�� | �ձ�������������Һ©�� | 100 mL����ƿ�����������ձ� |
|
|
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʼ��仯�����й㷺Ӧ�á�
(1)�����������Ϊ�����������֮����ȥ����ˮ���ӵIJ������������(�׳ơ��������ơ�)�dz��õ�ˮ���������仯ѧʽΪ________________��
(2)��������(NaH2PO2)�����ڻ�ѧ������
��NaH2PO2��PԪ�صĻ��ϼ�Ϊ_________��
�ڻ�ѧ��������Һ�к���Ni2����H2PO![]() �������������·���������Ӧ������ƽ��
�������������·���������Ӧ������ƽ��
____Ni2����____H2PO![]() ��____===____Ni����____H2PO
��____===____Ni����____H2PO![]() ��____
��____
(3)������뽹̿��ʯӢɰ��ϣ��ڵ�¯�м��ȵ�1 500 �����ɰ��ף���ӦΪ
2Ca3(PO4)2��6SiO2![]() 6CaSiO3��P4O10
6CaSiO3��P4O10
10C��P4O10![]() P4��10CO
P4��10CO
����Ӧ����31 g P4����Ӧ������ת�Ƶĵ�����Ϊ___________(��NA��ʾ�����ӵ�������ֵ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com