
 2HI(g)
2HI(g)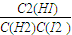 =
=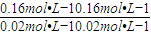
 2HI(g)
2HI(g)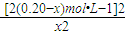 =64
=64 

 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物 A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
②A+RCOOH(或ROH)![]() 有香味的产物
有香味的产物
③1molA![]() 慢慢产生l.5mol气体
慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH3)为
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省四校高二(上)期末化学试卷(仙桃中学、麻城一中、新洲一中、武汉二中)(解析版) 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省黄冈市高一(下)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物 A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
②A+RCOOH(或ROH)![]() 有香味的产物
有香味的产物
③1molA![]() 慢慢产生l.5mol气体
慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH3)为
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com